Par le séquençage du génome, certains patients atteints de maladies auto-inflammatoires autrefois non diagnostiquées sont maintenant reconnus comme étant atteint d’un nouveau syndrome nommé VEXAS (vacuoles intracytoplasmiques dans les progéniteurs médullaires, E1 ubiquitine ligase, liée à l’X, syndrome auto-inflammatoire, mutation somatique).
Le syndrome VEXAS est causé par des mutations somatiques du gène UBA1 et le séquençage de ce gène constitue le test diagnostique de référence.
Les éléments à considérer pour envisager un syndrome VEXAS chez les patients présentant des symptômes autoinflammatoires sont des manifestations dermatologiques, un syndrome myélodysplasique ou une gammapathie monoclonale et une vacuolisation des précurseurs myéloïdes et érythroïdes dans la moelle osseuse.
Les avancées de la médecine génomique continueront à découvrir les causes de maladies non diagnostiquées jusqu’à maintenant.
Tout au long de l’histoire de la médecine, les progrès technologiques ont permis aux médecins de comprendre et de diagnostiquer des syndromes qui autrefois demeuraient des énigmes. Bien qu’Hippocrate décrivait déjà plusieurs caractéristiques de la tuberculose, il faudra attendre l’invention du microscope pour que les médecins comprennent qu’elle est causée par la bactérie Mycobacterium tuberculosis. De façon comparable, la technologie et l’application à la médecine du séquençage du génome (génomique) révolutionnent maintenant la compréhension de nombreuses maladies et de nombreux syndromes1.
En 2001, le premier essai de séquençage du génome humain dans son ensemble a pris plus de 5 ans; il est maintenant possible de générer des résultats applicables en pratique clinique à partir du séquençage du génome entier en aussi peu que 5 jours2. La foule de données générée par ces techniques a démontré que plusieurs maladies non diagnostiquées ont des origines génétiques spécifiques.
Nous illustrons la puissance de la génomique et son effet sur les diagnostics et la pratique cliniques grâce au syndrome VEXAS (vacuoles intracytoplasmiques dans les progéniteurs médullaires, E1 ubiquitine ligase, liée à l’X, syndrome auto-inflammatoire, mutation somatique) nouvellement découvert, qui a offert un diagnostic génétique unificateur à un groupe de patients atteints d’un syndrome auto-inflammatoire non diagnostiqué jusqu’à maintenant. Ce syndrome est pertinent pour de nombreux médecins puisqu’il peut se manifester par une vaste gamme de symptômes touchant plusieurs systèmes organiques, et ce, à l’âge adulte, ce qui démontre que des troubles d’origine génétique peuvent toucher presque tous les patients. Pour le moment, de nombreux patients atteints du syndrome VEXAS sont catégorisés selon des diagnostics existants et ils tireront avantage d’obtenir un diagnostic fondé sur les facteurs génétiques de leur maladie.
Que sont les syndromes auto-inflammatoires et comment se manifestent-ils?
On définit les syndromes auto-inflammatoires (aussi connus comme des maladies auto-inflammatoires systémiques) par la présence d’hyperactivation pathogène des mécanismes immunitaires de manière indépendante à la présence d’antigène. On a décrit plus de 40 problèmes de santé monogéniques distincts pouvant mener à un syndrome auto-inflammatoire3. Les caractéristiques exactes dépendent de la maladie en question, mais un tableau clinique fréquemment observé après des examens initiaux appropriés consiste en la présence d’une fièvre d’origine inconnue, définie comme une fièvre persistante (> 38,3°C pour > 3 semaines) sans cause évidente. Au cours d’une récente étude prospective réalisée aux Pays-Bas auprès de 73 patients atteints d’une fièvre d’origine inconnue, on a ciblé un syndrome auto-inflammatoire chez 22 % d’entre eux4. On devrait envisager les syndromes auto-inflammatoires chez les patients atteints d’une fièvre d’origine inconnue pour qui des examens approfondis ont exclu la possibilité d’une infection, d’un cancer, d’un syndrome hémophagocytaire et d’autres causes de fièvre et d’inflammation systémique.
Qu’est-ce que le syndrome VEXAS et quand devrait-on l’envisager comme diagnostic?
On a décrit pour la première fois le syndrome VEXAS en décembre 2020 après avoir procédé au séquençage de l’ensemble du génome d’une cohorte de patients dans le cadre du Programme des maladies non diagnostiquées des National Institutes of Health (NIH) aux États-Unis5. En intégrant des données de mutations génétiques à grande échelle à des informations sur les symptômes des patients, le NIH a ciblé 25 personnes dont les caractéristiques syndromiques étaient comparables et qui présentaient des mutations du gène UBA1 lié à l’X, lequel produit une enzyme qui joue un rôle important dans le recyclage des protéines à l’intérieur des cellules. On a confirmé que cette mutation était somatique (c.-à-d. acquise et non innée) et on a démontré qu’elle reproduit certaines caractéristiques du syndrome VEXAS lorsqu’elle est insérée dans le génome d’un modèle animal5. Peu après la publication de cet article déterminant, on a ciblé le premier cas de syndrome VEXAS au Canada6.
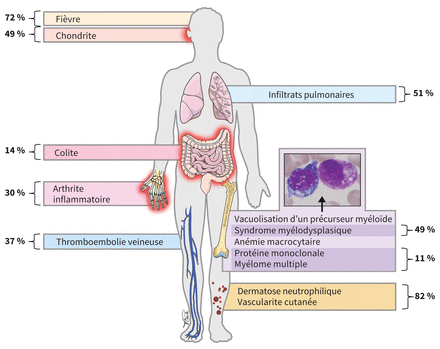
Le syndrome VEXAS est un syndrome auto-inflammatoire qui se manifeste à l’âge adulte en présentant plusieurs caractéristiques cliniques et pathologiques uniques qui le distinguent d’autres maladies rhumatologiques connues5. Les patients atteints de ce syndrome présentent à un âge avancé (âge médian de 71 ans) des symptômes comme de fortes fièvres récurrentes, des manifestations dermatologiques (p. ex., des dermatoses neutrophiliques, des vascularites cutanées), des chondrites de l’oreille et du nez, des infiltrats pulmonaires et des cytopénies (figure 1). Bien que ces manifestations soient les plus fréquentes, de récents rapports font état de symptômes additionnels qui lui sont associés, comme une uvéite, de l’inflammation ou des douleurs gastro-intestinales, une aortite et une hépatosplénomégalie7,10. Plusieurs patients atteints du syndrome VEXAS ont précédemment reçu un diagnostic de polychondrites récurrentes, de syndrome de Sweet ou de polyartérite noueuse. Puisque le syndrome VEXAS est une maladie liée à l’X, la plupart des patients sont de sexe masculin, mais on a aussi observé ce syndrome chez des patientes13. Les patients présentent souvent des symptômes graves et progressifs qui entraînent éventuellement une compromission de l’organe cible; 28 % des patients décrits dans une récente série sont décédés de leur maladie (tableau 1)5,7.
Les observations cliniques chez les patients atteints du syndrome VEXAS (vacuoles intracytoplasmiques dans les progéniteurs médullaires, E1 ubiquitine ligase, liée à l’X, syndrome auto-inflammatoire, mutation somatique) comprennent souvent de fortes fièvres, des manifestations dermatologiques (p. ex., des dermatoses neutrophiliques, des vascularites cutanées), des chondrites, des infiltrats pulmonaires, de l’anémie macrocytaire, un syndrome myélodysplasique ou une protéinémie monoclonale et une dépendance aux corticostéroïdes. La caractéristique de la vacuolisation des précurseurs myéloïdes est illustrée sur le panneau coulissant. La fréquence de chaque manifestation est notée en caractère gras5,7–12.
Image courtesy of Vicky Earle
Caractéristiques du syndrome VEXAS (vacuoles intracytoplasmiques dans les progéniteurs médullaires, E1 ubiquitine ligase, liée à l’X, syndrome auto-inflammatoire, mutation somatique) issu de cohortes ayant fait l’objet de publications*
Ce syndrome entraîne aussi des manifestations hématologiques caractéristiques. Presque tous les patients qui en sont atteints présentent une anémie macrocytaire et plusieurs ont un syndrome myélodysplasique concomitant de faible grade, une protéinémie monoclonale ou un myélome multiple. Ces patients arborent dans leur moelle osseuse des caractéristiques morphologiques qui sont hautement spécifiques à ce diagnostic, notamment une vacuolisation des précurseurs myéloïdes et érythroïdes. Ces caractéristiques peuvent ne pas être décrites dans les rapports de pathologie et un pathologiste devrait rechercher ces signes de façon spécifique chez les patients que l’on suspecte être atteints du syndrome VEXAS.
En raison du caractère récent de sa découverte, l’incidence et la prévalence de ce syndrome demeurent inconnues, bien que nous nous attendions à ce qu’il soit ciblé de façon plus fréquente une fois que la connaissance de ce diagnostic et l’accès au test seront davantage répandus.
Comment peut-on confirmer un diagnostic de syndrome VEXAS?
Les épreuves diagnostiques pour un patient chez lequel on suspecte la présence d’un syndrome VEXAS devraient comprendre l’examen des marqueurs inflammatoires (p. ex., protéines C-réactives, ferritine sérique), une biopsie de la moelle osseuse, des images des poumons, des épreuves fonctionnelles respiratoires ainsi que les examens nécessaires à l’élimination des diagnostics alternatifs. Cependant, le syndrome VEXAS peut seulement être confirmé par la présence d’une mutation somatique UBA1, habituellement en provenance du sang périphérique. Pour le moment, l’accès aux tests pour cette mutation est variable, en raison du caractère récent de la description du diagnostic. On devrait discuter de la disponibilité des tests avec des experts locaux qui ont examiné des patients atteints du syndrome VEXAS ou qui peuvent coordonner le séquençage du gène UBA1. On recommande de communiquer avec des hématologues ou des rhumatologues locaux qui présentent un intérêt pour les syndromes auto-inflammatoires ou le syndrome myélodysplasique. À l’avenir, un réseau canadien coordonné de professionnels détenant une expertise dans le syndrome VEXAS et les troubles qui y sont associés pourrait être utile.
Comment sont traités les patients atteints du syndrome VEXAS et par qui le sont-ils?
Les patients atteints du syndrome VEXAS dépendent généralement de stéroïdes et les corticostéroïdes sont habituellement la seule thérapie qui améliore de façon temporaire leurs symptômes inflammatoires. Étant donné que de nombreux patients auront fait une utilisation prolongée de stéroïdes pendant plusieurs années, des complications causées par l’usage à long terme de stéroïdes sont fréquentes et devraient être prises en compte lors de l’évaluation des modalités de traitement de ce syndrome (p. ex., une allogreffe de cellules souches hématopoïétiques). Des agents non stéroïdiens ou des antirhumatismaux modificateurs de la maladie sont inefficaces chez la plupart des patients atteints du syndrome VEXAS et les traitements ciblant les clones de cellules myéloïdes malignes constituent possiblement l’approche la plus efficace. Dans une étude récente, environ 50 % des patients atteints du syndrome VEXAS et d’un syndrome myélodysplasique concomitants et qui présentaient des symptômes inflammatoires hautement réfractaires ont vu leur état s’améliorer après un traitement à l’aide d’un agent hypométhylant, lequel constitue le traitement standard pour un syndrome myélodysplasique récurrent14. La seule thérapie présentant un potentiel curatif à long terme est l’allogreffe de cellules souches hématopoïétiques. Bien que celle-ci soit accompagnée de graves risques, la greffe s’est révélée un succès chez de nombreux patients15 et un essai clinique de phase 2 est en cours (ClinicalTrials.gov, numéro d’enregistrement NCT05027945). Prochainement, les connaissances en lien avec l’efficacité des traitements pour les patients atteints du syndrome VEXAS évolueront probablement rapidement.
On devrait prendre ces patients en charge à l’aide d’une approche multidisciplinaire, en intégrant généralement des rhumatologues, des hématologues et des spécialistes des maladies infectieuses. On devrait déterminer l’admissibilité à l’allogreffe de cellules souches hématopoïétiques de façon précoce dans le parcours de la maladie puisque les complications reliées au syndrome VEXAS (p. ex., une fibrose pulmonaire avancée, des infections persistantes) peuvent éventuellement limiter cette option thérapeutique.
De quelle manière la médecine génomique pourra-t-elle influencer la pratique à l’avenir?
La découverte du syndrome VEXAS constitue un exemple de la manière dont la génomique pourra redéfinir plusieurs aspects de la pratique médicale à l’avenir. Dans certains domaines, comme l’hématologie et l’oncologie, l’utilisation de plateformes de séquençage génétique se pratique couramment et est devenue la norme thérapeutique pour plusieurs patients. Plus on comprendra les contributions des altérations génétiques aux maladies humaines, plus la médecine génomique sera intégrée à la pratique clinique.
Le JAMC vous invite à soumettre vos textes pour la rubrique « Innovations » qui met en évidence les récentes avancées diagnostiques et thérapeutiques. De nouvelles utilisations de traitements existants seront également considérées. Pour la publication, les avantages de l’innovation, sa disponibilité et ses limites doivent être mis en évidence clairement, mais brièvement. Les éléments visuels (images) sont essentiels. Veuillez soumettre de brefs articles factuels (1000 mots et 5 références maximum) en ligne au http://mc.manuscriptcentral.com/cmaj ou envoyez un courriel à andreas. laupacis{at}cmaj.ca pour échanger des idées.
Footnotes
Intérêts concurrents: Luke Chen mentionne des honoraires de conférenciers de la société GlaxoSmithKline, indépendamment des travaux soumis. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement du patient.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception de l’étude ainsi qu’à l’ébauche du manuscrit, ont révisé de façon critique, ont donné leur approbation à la version finale destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
Soutien financier: Ryan Stubbins est soutenu par des subventions provenant de la Société de leucémie et lymphome du Canada, les Instituts de recherche en santé du Canada (202002LFC-439884) et le Programme des cliniciens-chercheurs de l’Université de la Colombie-Britannique.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/