La bérylliose est une réaction d’hypersensibilité de type IV, acquise à la suite d’une exposition au béryllium, généralement dans un contexte professionnel.
La bérylliose présente des symptômes respiratoires non spécifiques, dont l’essoufflement et une toux sèche, qui ressemblent à ceux d’autres affections, en particulier la sarcoïdose.
Il faut obtenir les antécédents professionnels de la patientèle dans la recherche exploratrice de symptômes respiratoires.
Le test de prolifération lymphocytaire au béryllium est le seul examen de diagnostic actuellement capable de différencier la bérylliose de la sarcoïdose.
Une femme de 56 ans a consulté son médecin de famille en raison d’un essoufflement insidieux qui progressait depuis plusieurs mois et qui était passé de la dyspnée d’effort à l’essoufflement au repos. Elle n’avait pas de fièvre, de sueurs nocturnes, de perte de poids ni d’hémoptysie, et était par ailleurs asymptomatique. Au moment de la consultation, ses antécédents médicaux comprenaient l’apnée du sommeil et un trouble de l’humeur, lequel était traité par un inhibiteur de la recapture de la sérotonine et de la noradrénaline. Elle n’avait jamais fumé. Elle travaillait comme soudeuse depuis plus de 30 ans dans le secteur du pétrole et du gaz. Elle utilisait diverses méthodes de soudure et divers métaux, dont certains qu’elle qualifiait de « métaux exotiques », dans des installations intérieures et extérieures mal aérées. Elle portait un appareil de protection respiratoire à l’occasion. Son médecin de famille l’a envoyée en pneumologie à l’hôpital régional pour d’autres examens (tableau 1). Les intervalles entre les examens sont dus en partie à des déménagements d’une province à l’autre durant le processus.
Résumé des examens chez une soudeuse de 56 ans, et diagnostics différentiels associés
Une épreuve fonctionnelle respiratoire a indiqué une légère diminution de la capacité de diffusion, observation pouvant correspondre à plusieurs diagnostics possibles (tableau 2). Les résultats de la formule sanguine complète, de l’épreuve de coagulation, de l’épreuve fonctionnelle hépatique, de l’analyse des électrolytes, de l’épreuve fonctionnelle rénale et de la mesure du taux de thyréostimuline étaient normaux. Une radiographie pulmonaire a révélé une atélectasie sous-segmentaire non spécifique dans la zone inférieure gauche des poumons. Une tomodensitométrie des poumons a montré plusieurs nodules pulmonaires non calcifiés de 2 à 3 mm, ainsi qu’un nodule mal défini à l’aspect de verre dépoli de 18 mm dans le lobe inférieur gauche et un nodule de 7 mm dans le lobe supérieur droit. Les nœuds lymphoïdes du hile et du médiastin étaient légèrement proéminents, mais pas au-delà des limites normales. Nous n’avons pas observé de marques réticulaires, d’épaississement anormal de septums, d’emphysème, de perte de volume ni d’épanchement pleural. Les résultats de l’imagerie semblaient indiquer une infection granulomateuse antérieure, une maladie pulmonaire interstitielle ou une tumeur maligne.
Résultats des épreuves fonctionnelles respiratoires
Au cours des 6 mois suivants, 3 ensembles de biopsies transbronchiques des poumons et des nœuds lymphoïdes ont été recueillis par bronchoscopie sans fluoroscopie. Les premières biopsies ont montré des tissus normaux sans signes d’infection. Comme les maladies inflammatoires sont connues pour l’hétérogénéité des granulomes, il est pratique courante de procéder à de nouveaux prélèvements en cas de doute raisonnable. Les deuxièmes biopsies étaient de qualité sous-optimale. Nous avons donc obtenu un troisième ensemble de biopsies, qui a montré des granulomes non caséeux, circonscrits dans le tissu pulmonaire et les nœuds lymphoïdes (figure 1). Ces dernières biopsies étaient négatives à l’égard des bacilles acidorésistants (coloration de Ziehl–Neelsen), des champignons (coloration à la méthénamine d’argent de Grocott) et des matières étrangères polarisables. Les autres examens de recherche d’infection, dont un lavage bronchoalvéolaire, par des colorations et des cultures bactériennes et mycobactériennes de pratique courante, étaient négatifs. Le diagnostic différentiel indiquait une maladie pulmonaire interstitielle inflammatoire.
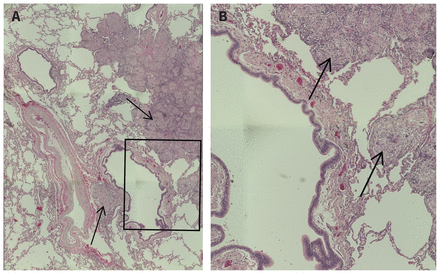
Granulomes non nécrosants, circonscrits, prélevés dans le lobe inférieur gauche des poumons chez une femme de 56 ans. (A) Grossissement de faible puissance du tissu pulmonaire avec granulomes (flèches) autour des faisceaux bronchovasculaires et des septums interlobulaires (grossissement original × 100); (B) Grossissement de forte puissance d’une région particulière du tissu pulmonaire (région encadrée dans l’image A) avec granulomes (flèches) (grossissement original × 200).
Pour faire la distinction entre les 2 principales causes présumées de maladie pulmonaire interstitielle, la sarcoïdose et la bérylliose, nous avons fait un test de prolifération lymphocytaire au béryllium (BeLPT) par lavage bronchoalvéolaire. Les résultats ont indiqué une relation dose–réponse de la prolifération des lymphocytes au sulfate de béryllium, ce qui signait le diagnostic de bérylliose (tableau 3). La patiente s’est donc réorientée vers une nouvelle carrière (camionneuse), la solution la plus simple afin de réduire au minimum et en toute confiance son exposition au béryllium. Étant donné l’atteinte pulmonaire minimale au moment du diagnostic ainsi que le retrait de son travail de soudure, aucun traitement pharmacologique n’a été prescrit.
Résultats du test de prolifération lymphocytaire au béryllium par lavage bronchoalvéolaire
Nous avons surveillé le fonctionnement pulmonaire durant l’année suivante à l’aide de 3 épreuves fonctionnelles respiratoires, qui ont révélé une aggravation, puis une amélioration de la capacité de diffusion (tableau 1). Neuf mois après le diagnostic, la patiente a connu un épisode de malaise thoracique migratoire et d’essoufflement, qui s’est résorbé spontanément; une scintigraphie pulmonaire de perfusion avec ventilation n’a montré aucun embole pulmonaire. Nous avons recommandé un suivi régulier avec son médecin de famille pour surveiller la réapparition des symptômes respiratoires, et une épreuve fonctionnelle respiratoire annuelle jusqu’à l’atteinte d’une bonne stabilisation des résultats.
Discussion
Le béryllium est un métal de faible poids moléculaire, grandement utilisé, seul ou dans des alliages, en raison de ses propriétés qui se prêtent bien à la soudure1. L’exposition au métal se produit la plupart du temps sur les lieux de travail; les secteurs à haut risque comprennent la construction (soudure, projection d’abrasif), l’automobile, la céramique, le recyclage de cartes de circuit informatiques, l’électronique, l’exploitation du pétrole et du gaz, la réparation de la machinerie industrielle, la bijouterie, la transformation des métaux et l’exploitation minière1.
Exposition professionnelle
L’exposition professionnelle au béryllium se produit principalement par l’inhalation de particules aéroportées1. Il n’existe actuellement aucun niveau sécuritaire d’exposition au béryllium, métal désigné cancérogène pour les humains (groupe 1) par le Centre international de recherche sur le cancer2. Le seuil actuellement établi par l’association American Conference of Governmental Industrial Hygienists pour le béryllium est de 0,05 μg/m3 d’air sur les lieux de travail, ce qui correspond à la concentration moyenne de particules qu’une personne en bonne santé pourrait inhaler par quart de travail au cours de sa carrière sans effets néfastes pour la santé2. La soudure est connue pour son risque élevé d’exposition au béryllium : d’après une étude portant sur divers secteurs industriels, les soudeurs et soudeuses avaient une exposition moyenne pondérée sur 8 heures, équivalente à 0,24 μg/m3 au cours de leur quart de travail complet3. Le port d’un demi-masque respiratoire à filtre de particules P100 (qui filtre 99,97 % de toutes les particules) permet de réduire l’exposition à 0,024 μg/m3, soit en deçà de la plupart des limites canadiennes d’exposition professionnelle (0,05 μg/m3). Les employeurs et employeuses ont l’obligation légale de s’assurer que les risques professionnels sont adéquatement contenus en mettant en œuvre des mesures préventives qui suivent une séquence particulière (tableau 4).
Mesures de prévention pour réduire au minimum l’exposition professionnelle au béryllium
Conséquences et manifestations cliniques de l’exposition
L’exposition au béryllium cause principalement la sensibilisation au béryllium et la bérylliose (aussi appelée bérylliose pulmonaire chronique), 2 formes de réaction d’hypersensibilité de type IV, acquise à la suite d’une exposition au béryllium. La sensibilisation au béryllium ressemble à la bérylliose, mais sans atteinte pulmonaire. La bérylliose cause une maladie pulmonaire interstitielle granulomateuse, accompagnée d’une inflammation transitoire et de granulomes4. Les manifestations cliniques des 2 affections sont principalement un essoufflement non caractéristique et une toux sèche; la fièvre, les sueurs nocturnes, l’hippocratisme et la perte de poids sont moins fréquents4. Les symptômes s’atténuent généralement après la fin de l’exposition. Le polymorphisme du gène HLA-DPB1 avec acide glutamique au 69e codon est associé à un risque de bérylliose jusqu’à 8 fois supérieur à la normale chez la patientèle ayant des antécédents d’exposition au béryllium; sa prévalence est de 15 % à 25 % dans la population générale4,5. En pratique, le dépistage génétique des groupes professionnels à haut risque n’est pas fait systématiquement, en raison de problèmes éthiques entourant la discrimination liée à l’emploi et aux assurances.
Prévalence, facteurs de risque et pronostic
Les cas déclarés de bérylliose sont limités, vieux et vraisemblablement sous-documentés6. La prévalence de la bérylliose dans les populations exposées au béryllium est estimée entre 2 % et 5 %, mais pourrait atteindre 15 % chez les travailleurs et travailleuses des secteurs à forte exposition, comme les machinistes7. Puisque la bérylliose ressemble sur les plans clinique, pathologique et radiologique à la sarcoïdose, on estime qu’environ 6 % de la patientèle chez qui un diagnostic de sarcoïdose a été posé souffrirait plutôt de bérylliose6. La probabilité s’élève à 40 % quand l’exposition au béryllium est établie6. La prévalence de la sarcoïdose en 2015, en Ontario, était de 143 cas pour 100 000 personnes, ce qui donne à penser que la prévalence de la bérylliose pourrait atteindre 8 cas pour 100 000 dans la population générale, voire plus dans certaines populations de travailleurs et travailleuses8.
Le principal facteur de risque de la bérylliose est l’exposition au béryllium. Le temps écoulé entre la sensibilisation au métal et l’apparition des symptômes après l’exposition peut varier de 3 semaines à 30 ans1. La gravité de la bérylliose et le pronostic sont variables, mais sont pires lorsque l’intensité d’exposition est élevée, lorsque les métaux utilisés contiennent un fort pourcentage de béryllium et lorsqu’il y a un grand nombre de lymphocytes dans les échantillons de lavage bronchoalvéolaire9. Si les symptômes diminuent après la fin de l’exposition à l’agent sensibilisant ou le traitement pharmacologique, cette amélioration se poursuit généralement tant que l’évitement ou le traitement continuent. Malgré le traitement, certains patients et patientes finissent par souffrir de fibrose pulmonaire. Dans une étude de cohorte, 8 personnes atteintes de bérylliose présentaient des signes de fibrose pulmonaire avant le traitement; la fibrose chez 6 d’entre elles n’a pas évolué durant le traitement par les corticostéroïdes4.
Examens
Les examens non spécifiques de la bérylliose comprennent les épreuves fonctionnelles respiratoires et l’imagerie des poumons, qui peuvent révéler une diminution de la capacité de diffusion et une lymphadénopathie périlymphatique avec ou sans nodules pulmonaires à l’aspect de verre dépoli, respectivement. L’exploration initiale de la sensibilité au béryllium peut être faite au moyen de 2 tests BeLPT de sang périphérique (sensibilité de 68,3 %; spécificité de 96,9 %); 2 échantillons sont prélevés simultanément en raison de la faible sensibilité de l’analyse et des critères diagnostiques1,10. Si les 2 résultats sont négatifs, on peut surveiller les symptômes respiratoires, demander des épreuves fonctionnelles respiratoires et suivre la sensibilisation au béryllium (par BeLPT sérique) chez la patientèle à risque élevé1. Si les résultats sont négatifs ou ambigus et qu’on soupçonne encore la bérylliose, un BeLPT par lavage bronchoalvéolaire confirmera souvent le diagnostic1. Cet examen peut être préférable en première intention lorsque les épreuves fonctionnelles respiratoires ou l’imagerie des poumons sont anormales1.
Pour diagnostiquer la bérylliose, il doit y avoir des antécédents d’exposition au béryllium, des résultats histopathologiques correspondant à la bérylliose (granulomes non caséeux) et un BeLPT positif (sérique ou par lavage bronchoalvéolaire) 1. Les biopsies pulmonaires ont un taux de faux négatifs de 5 %–10 % et peuvent nécessiter un nouveau prélèvement11. Le BeLPT peut permettre de distinguer la sarcoïdose de la bérylliose, alors que la plupart des autres résultats seront semblables. Le BeLPT fournit aussi la numération des lymphocytes dans les échantillons de sérum ou de liquide de lavage bronchoalvéolaire après une exposition au béryllium. Un résultat positif à l’analyse indique une prolifération exagérée des lymphocytes en réaction au béryllium. Au National Jewish Health, un hôpital situé au Colorado, on effectue la plupart des BeLPT par lavage bronchoalvéolaire en Amérique du Nord, pour une sensibilité égale ou supérieure à 97,2 %12.
Prise en charge et prévention secondaire
Les glucocorticoïdes oraux sont le traitement pharmacologique de première intention de la bérylliose; on commence par une dose quotidienne de 20–40 mg pendant 3 mois, qu’on réduit ensuite de 5 mg par semaine jusqu’à la plus faible dose efficace11. Les régimes posologiques des glucocorticoïdes reposent sur un petit nombre de rapports et de séries de cas4. Le méthotrexate est utilisé chez la patientèle intolérante ou réfractaire aux glucocorticoïdes; on commence par une dose 7,5 mg par semaine, qu’on augmente ensuite de 2,5 mg toutes les 2 semaines jusqu’à une dose de 15 mg par semaine11. L’utilisation du méthotrexate est fondée sur son usage dans le traitement de la sarcoïdose11. La prise en charge de la bérylliose devrait prioriser l’élimination de l’exposition professionnelle par la réaffectation (tableau 4). En pratique, l’exposition est en grande partie limitée par les appareils de protection respiratoire. Généralement, les demi-masques respiratoires à filtre P100 suffisent s’ils sont bien ajustés et toujours utilisés correctement.
Les professionnelles et professionnels de la santé devraient envisager une cause professionnelle aux symptômes respiratoires lorsqu’il y a de l’essoufflement ou de la toux. La collecte de renseignements sur l’ensemble des antécédents professionnels comprend l’exploration des associations symptômes–lieux de travail, du potentiel d’exposition, des tâches et des mesures de prévention (tableau 5). L’exercice est particulièrement important chez la patientèle chez qui on soupçonne la présence ou on a posé un diagnostic de sarcoïdose.
Renseignements essentiels à l’analyse des antécédents professionnels respiratoires
La section « Études de cas » présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares, ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs : www.cmaj.ca
Footnotes
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement de la patiente.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception du travail. Matthew Loss a rédigé la version préliminaire du manuscrit. Tous les auteurs ont révisé de manière critique le contenu intellectuel important, ont donné leur approbation finale à la version destinée à être publiée et ont accepté d’être responsables de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/