Voir la version anglaise de l’article ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.220936; pour connaître le point de vue d’une personne atteinte de polyradiculoneuropathie inflammatoire démyélinisante, voir www.cmaj.ca/lookup/doi/10.1503/cmaj.230085-f
La polyneuropathie est une maladie neurologique courante dont il existe plusieurs sous-types affectant les fibres motrices, sensorielles ou autonomes.
La polyneuropathie symétrique distale est le sous-type le plus courant de polyneuropathie; elle se présente habituellement sous forme de signes et symptômes principalement sensoriels et dépend de la longueur des fibres affectées.
Les caractéristiques cliniques, telles qu’un déclenchement aigu ou subaigu, l’asymétrie, la non-dépendance à l’égard de la longueur des fibres, les signes surtout moteurs et les caractéristiques systémiques associées, justifient une demande de consultation en médecine neuromusculaire pour un examen plus approfondi de la polyneuropathie.
La plupart des causes de la polyneuropathie symétrique distale sont identifiables par l’analyse des antécédents médicaux; certaines causes sont identifiables à l’aide d’analyses de laboratoire de dépistage.
Les options thérapeutiques orales de première intention pour les symptômes de la neuropathie diabétique douloureuse sont les antidépresseurs tricycliques, les inhibiteurs de la recapture de la sérotonine et de la noradrénaline, les anticalciques et les gabapentinoïdes, qui semblent tous dotés d’une efficacité similaire.
La polyneuropathie est une maladie neurologique commune dont la prévalence dans la population générale est d’environ 1 %–3 %, et passe à environ 7 % chez les personnes de plus de 65 ans1. La polyneuropathie a plusieurs étiologies et peut se manifester de différentes façons; c’est pourquoi il faut appliquer une approche clinique rationnelle à son évaluation, à son diagnostic et à sa prise en charge. Nous passons ici en revue l’évaluation de la polyneuropathie en soulignant les aspects importants de l’anamnèse et de l’examen neurologique. Nous insistons sur le rôle des épreuves diagnostiques pour la polyneuropathie symétrique distale (PSD), le sous-type le plus commun, et proposons une approche au traitement des symptômes de la polyneuropathie diabétique douloureuse (PDD). Nous nous inspirons, autant que possible, de lignes directrices en matière de pratique clinique, de méta-analyses et de revues systématiques, puisqu’il s’agit des données probantes de la meilleure qualité (encadré 1).
Encadré 1: Stratégie d’interrogation pour cette revue
À l’aide de PubMed, nous avons recensé toutes les publications des 10 dernières années sur la prise en charge de la polyneuropathie en médecine de soins primaires ou en médecine d’urgence à partir des termes en langue anglaise « polyneuropathy », « peripheral neuropathy » et « management ». Nous avons passé en revue celles qui étaient pertinentes en accordant la priorité aux lignes directrices en matière de pratique clinique, aux méta-analyses et aux revues. Dans le cas des lignes directrices en matière de pratique clinique, nous avons étendu la recherche aux 20 dernières années et passé en revue les listes bibliographiques de chacune pour pouvoir les inclure au besoin.
Quelles sont les caractéristiques cliniques de la polyneuropathie?
Les symptômes de polyneuropathie se classent selon que les fibres nerveuses touchées sont sensorielles, motrices ou autonomes. Les fibres sensorielles incluent les fibres de grand calibre, qui traitent les sensations vibratoires et la proprioception, et les fibres de petit calibre, qui traitent les signaux douloureux et les signaux thermiques. Les 2 modalités doivent être examinées parce que leur atteinte relative donne un indice de la cause. La dysfonction de l’un ou l’autre des types de fibres sensorielles peut entraîner une altération sensorielle qui va des paresthésies, manifestées par des picotements (symptômes sensoriels positifs), à des pertes de sensibilité substantielles, voire complètes, connues sous les termes d’hypoesthésie et d’anesthésie (symptômes sensoriels négatifs). La dysfonction sensorielle des fibres longues peut entraîner un trouble de la démarche causé par la perte de proprioception (ataxie sensorielle). La dysfonction sensorielle des petites fibres entraîne le plus souvent de la douleur, et dans certains cas, une hyperesthésie, soit une sensation accrue des stimulations tactiles, ou une allodynie, une perception douloureuse lors de stimuli normalement indolores. Les épisodes spontanés de douleur s’accompagnent parfois de rougeur et d’enflure à la zone cutanée affectée en raison de la transmission de signaux douloureux non provoqués par les fibres C sensorielles endommagées qui libèrent également des substances vasoactives à l’origine d’une inflammation neurogène2. Parmi les autres symptômes associés aux petites fibres sensorielles, mentionnons douleurs profondes, malaise à l’effort, et démangeaisons neuropathiques3. En revanche, quand ce sont les fibres motrices qui sont atteintes, on décrit d’abord une sensation de faiblesse qui peut se manifester comme une perte de dextérité, un trouble de la démarche ou les deux. Les symptômes autonomes causés par la neuropathie passent parfois inaperçus parce qu’ils peuvent avoir de nombreuses autres causes. Les symptômes autonomes courants incluent intolérance orthostatique, gastroparésie, constipation, diarrhée, vessie neurogène, troubles sexuels, symptômes pupillomoteurs (tels que vision trouble) et symptômes vasomoteurs qui peuvent entraîner une sécheresse oculaire, buccale ou cutanée ou une sensation de brûlure ou de rougeur cutanée4.
La polyneuropathie symétrique distale est le sous-type de polyneuropathie le plus courant; elle se caractérise par un processus dépendant de la longueur des fibres, les plus longues étant affectées d’abord. Les signes incluent une faiblesse symétrique distale avec perte sensorielle (petites fibres, longues fibres, ou les deux) et perte ou émoussement des réflexes de la cheville5. La perte sensorielle commence par les pieds, sans lien avec le dermatome et selon une distribution polyneuropathique5. Lorsque les symptômes ou les signes sensoriels atteignent la partie supérieure du mollet, l’extrémité des doigts est affectée puisque la longueur des nerfs dans ces régions est grosso modo équivalente. C’est ce que l’on appelle une distribution de la perte sensorielle en « gants et chaussettes »6. Dans les cas graves, cela est suivi d’une perte sensorielle au niveau de la portion moyenne antérieure du thorax et de l’abdomen, causée par la dégénérescence distale des nerfs intercostaux thoraciques. Une faiblesse fait suite à la perte sensorielle, affectant d’abord l’extension des orteils puis la dorsiflexion de la cheville6. Des symptômes autonomes peuvent survenir si les petites fibres sensorielles sont aussi touchées; elles débutent généralement à la portion distale, avec des anomalies de la sudation ou une instabilité circulatoire pédieuse5.
Les médecins doivent connaître les maladies qui pourraient ressembler à la polyneuropathie, particulièrement la myélopathie cervicale, qui peut se manifester par une distribution pyramidale de la faiblesse (c.à-d., faiblesse préférentielle des extenseurs des membres supérieurs et des fléchisseurs des membres inférieurs), l’hyperréflexie en aval de la lésion, un niveau sensoriel et une dysfonction vésicale et intestinale. Les causes immédiates de la myélopathie, y compris la compression de la moelle épinière ou l’infarctus ischémique, peuvent s’accompagner d’une perte de réflexe au niveau de la lésion ou en aval de celle-ci.
Comment évalue-t-on les cas?
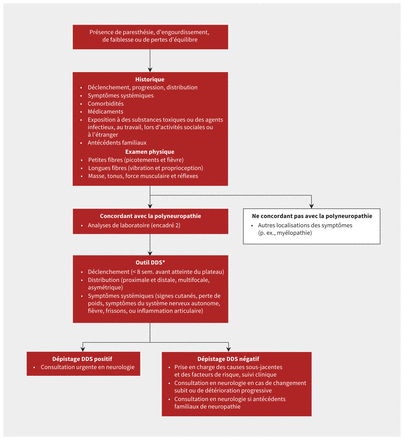
Une approche à l’évaluation clinique des cas possibles de polyneuropathie et un guide de sélection des cas qui nécessitent une consultation urgente en médecine de spécialité sont décrits à la figure 1. En présence de certains signes et symptômes, une consultation urgente s’impose et il est important de reconnaître les sous-types de polyneuropathie et les diagnostics différentiels principaux afin d’en orienter la prise en charge.
Approche à l’évaluation d’une polyneuropathie présumée. *Des résultats positifs avec l’outil de dépistage DDS accroissent la probabilité d’une cause inflammatoire ou d’une autre neuropathie traitable. Remarque: DDS = déclenchement, distribution et caractéristiques systémiques.
Les cas de neuropathie qui débutent de manière aiguë (en quelques jours) ou subaiguë (en quelques semaines) avec atteinte d’un plateau (stabilité des déficits neurologiques accumulés) en l’espace de 8 semaines suivant le déclenchement des symptômes requièrent une consultation urgente auprès de spécialistes en médecine neuromusculaire7. Cela s’applique aussi aux neuropathies périphériques dont le déclenchement des symptômes est hyperaigu (p. ex., chute du poignet ou du pied) puisqu’il y a un risque d’atteinte vasculaire. La neuropathie aiguë qui s’accompagne d’une douleur substantielle ou d’un traumatisme associé pourrait nécessiter une prise en charge au service des urgences.
D’autres modes de présentation font fortement penser à la neuropathie vasculaire, notamment la polyneuropathie douloureuse à progression rapide et les mononeuropathies multiples (mononévrites multiplex); la mononeuropathie se définit alors par la présence de signes et symptômes attribuables à 1 seul nerf8. Un mode de présentation non dépendant de la longueur des fibres, accompagné de faiblesse proximale et distale, pourrait évoquer un processus de démyélinisation inflammatoire, comme la polyradiculoneuropathie démyélinisante inflammatoire chronique (PDIC), particulièrement si les déficits moteurs sont d’une ampleur comparable ou supérieure à celle des déficits sensoriels. Une neuropathie diabétique moins courante, la radiculoplexopathie lombo-sacrée, est une neuropathie douloureuse asymétrique des membres inférieurs qui évolue rapidement et peut causer une morbidité importante.
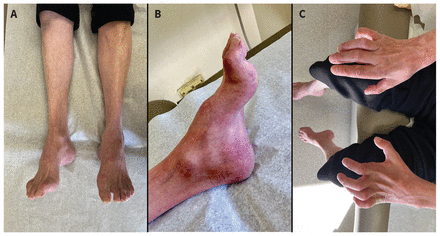
Les diagnostics différentiels des sous-types de polyneuropathie sont énumérés au tableau 1. Une aréflexie diffuse sans autre déficit neurologique à l’examen neurologique peut nécessiter une demande de consultation, compte tenu du risque de cause héréditaire. Les réflexes asymétriques isolés, comme la perte de réflexe de 1 des 2 chevilles, peuvent évoquer une mononeuropathie ou une radiculopathie pour lesquelles une demande de consultation non urgente pour une évaluation neuromusculaire serait appropriée. L’atrophie de la partie distale du mollet, les orteils en marteau et le pied creux (cambrure du pied prononcée) sont caractéristiques d’une neuropathie de longue date, qui s’observe souvent en présence de neuropathies héréditaires (figure 2).
Diagnostics différentiels des sous-types de polyneuropathie9
Clichés d’un patient atteint de polyneuropathie chronique liée à la maladie de Charcot–Marie–Tooth, avec signes (A) d’atrophie distale des muscles de la jambe et du pied; (B) de pied creux (cambrure prononcée), orteils en marteau et coloration anormale de la peau des pieds; et (C) de grave atrophie des muscles intrinsèques de la main (y compris des muscles lombricaux) avec préservation relative des muscles de l’avant-bras, entraînant une hyperextension métacarpophalangienne et une flexion interphalangienne proximale et distale connue sous le nom de « main en griffes ».
Un outil de dépistage comportant des éléments relatifs au déclenchement, à la distribution et aux caractéristiques systémiques (DDS) peut servir à identifier clairement les neuropathies inflammatoires. Ce genre d’outil donne un résultat positif en présence de 1 ou plus des caractéristiques suivantes: déclenchement aigu ou subaigu (< 8 semaines avant l’atteinte du plateau), distribution non liée à la longueur des fibres ou au moins 1 signe systémique (signes cutanés, perte de poids, symptômes du système nerveux autonome, fièvre et frissons ou inflammation articulaire)7. L’outil de dépistage a une sensibilité de 96 % et une spécificité de 85 % pour ce qui est de reconnaître les neuropathies inflammatoires, y compris le syndrome de Guillain–Barré, la PDIC (et ses sous-types), les neuropathies motrices multifocales, les neuropathies vasculaires et les neuropathies paranéoplasiques7. Les signes systémiques d’une neuropathie axonale justifieraient aussi une demande de consultation en médecine neuromusculaire. La reconnaissance et le traitement rapides sont importants puisque les neuropathies laissées sans traitement adéquat peuvent entraîner une grave morbidité.
Des examens électrophysiologiques peuvent aider au diagnostic et orienter la prise en charge et le suivi clinique. Dans bien des régions du Canada, il est difficile d’accéder rapidement à des spécialistes en médecine neuromusculaire et les demandes de consultation sont adressées à la neurologie générale. Si l’on soupçonne un syndrome de Guillain–Barré, il faut se diriger vers le service des urgences local pour examen et possible hospitalisation en raison du risque de faiblesse progressive, d’insuffisance respiratoire et de dysautonomie. L’évaluation électrodiagnostique urgente est indiquée puisqu’elle peut confirmer le diagnostic et orienter la prise en charge de façon spécifique et définitive10.
Quelles épreuves facilitent le diagnostic de la polyneuropathie symétrique distale?
La présence de signes et symptômes neuropathiques et les résultats électrodiagnostiques procurent le plus haut niveau d’exactitude du diagnostic de PSD5. Les observations à l’examen physique incluent absence ou émoussement des réflexes de la cheville, diminution de la sensation distale et faiblesse ou atrophie musculaire distale. Les symptômes neuropathiques seuls confèrent une précision diagnostique relativement faible; les signes sont de meilleurs prédicteurs et il faut leur accorder plus de poids5. Les examens électrodiagnostiques procurent un niveau élevé de spécificité pour ce qui est du diagnostic clinique11,12.
On ignore s’il faut soumettre tous les cas de PSD présumés à des examens électrodiagnostiques. Quatre études d’observation ont révélé que l’évaluation électrodiagnostique était associée à une modification du diagnostic, de la prise en charge ou des deux dans 40 % des cas, mais seulement 1 étude a porté sur les demandes de consultation pour PSD13–16. Par contre, une étude de cohorte rétrospective a permis d’observer un changement de la prise en charge chez moins de 1 % des cas de PSD observés en neurologie communautaire17. Ces observations contradictoires témoignent probablement de l’exclusion de plusieurs autres types de neuropathies lors de cette étude puisque plus de 80 % des participants souffraient d’une neuropathie attribuée à une anomalie du métabolisme du glucose18.
Nous suggérons un examen électrodiagnostique dans la plupart des cas de polyneuropathie, y compris la PSD, surtout si l’étiologie n’a pas été établie. Les examens de conduction nerveuse et l’électromyographie permettent de catégoriser la polyneuropathie selon qu’elle est principalement axonale ou démyélinisante, motrice, sensorielle ou les deux, et acquise ou héréditaire. Toutes ces catégories jouent un rôle important dans la détermination de la cause et la prise en charge9. Par exemple, la polyneuropathie symétrique démyélinisante distale acquise, une variante de la PDIC, peut faire penser à la PSD, mais requiert des examens ciblés et un traitement d’immunothérapie19. Les examens de conduction nerveuse et l’électromyographie fournissent également d’autres renseignements utiles, notamment la chronicité, le pronostic et, dans certains cas, la réponse au traitement.
La neuropathie sensorielle des petites fibres uniquement s’accompagnera de résultats normaux aux examens électrodiagnostiques parce que ces tests n’évaluent que le fonctionnement des fibres motrices et sensorielles longues. La biopsie cutanée et la mesure de la densité des fibres nerveuses intraépidermiques sont des marqueurs validés et reproductibles de la pathologie sensorielle liée aux petites fibres20. Il s’agit de l’examen standard pour le diagnostic de la neuropathie des petites fibres recommandé par l’Académie américaine de neurologie (AAN), avec une sensibilité de 45 %–90 % et une spécificité de 95 %–97 %21. Toutefois, sa disponibilité et son remboursement varient considérablement au Canada, ce qui en limite l’utilisation. Les lignes directrices en matière de pratique clinique de l’AAN recommandent aussi aux médecins d’envisager des épreuves du système autonome (c.à-d., épreuves sudomotrices, cardiovagales et vasomotrices adrénergiques) lorsqu’on soupçonne des neuropathies autonomes et des neuropathies sensorielles des petites fibres21. La biopsie nerveuse est utile lorsqu’on soupçonne la vascularite, la sarcoïdose et les maladies infiltrantes (comme le cancer ou l’amyloïdose).
Comment détermine-t-on l’étiologie d’une polyneuropathie symétrique distale acquise?
L’anamnèse et l’examen neurologique sont déterminants pour cerner l’étiologie de la PSD. Dans l’ensemble, on établira la cause après l’anamnèse et l’examen physique pour la PSD dans 60 % des cas; les analyses de laboratoire de dépistage peuvent révéler la cause dans un autre 10 % des cas, et environ 30 % des cas demeurent idiopathiques6,22,23. On parle de neuropathie axonale idiopathique chronique en présence de polyneuropathie à progression lente chez des individus ambulatoires généralement âgés de plus de 60 ans24.
Les causes fréquentes de la PSD incluent le diabète, les troubles liés à la consommation d’alcool, l’insuffisance rénale et la prise de médicaments, y compris la chimiothérapie; le diabète en est la cause la plus fréquente (tableau 2)26. Environ 40 %–50 % des cas de diabète présenteront une neuropathie détectable dans les 10 années qui en suivent le déclenchement27. Toutefois, d’autres causes traitables de PSD doivent quand même être envisagées chez cette population27–29. La neuropathie liée à la prise d’alcool est une PSD à progression lente irréversible, probablement médiée par un ensemble d’effets toxiques directs et par un déficit vitaminique secondaire, par exemple en vitamine B1 ou B12 25. La neuropathie urémique s’observe chez jusqu’à 90 % des personnes qui ont une vitesse de filtration glomérulaire inférieure à 6 mL/min/1,73 m2 30. Certains médicaments et agents de chimiothérapie peuvent aussi provoquer la PSD (tableau 2).
Médicaments d’usage courant associés à la polyneuropathie25
Des analyses de laboratoire de dépistage sont habituellement utilisées dans les cas de PSD pour identifier les causes traitables. Les lignes directrices en matière de pratique clinique de l’AAN recommandent des analyses de laboratoire de dépistage de haut rendement pour tous les cas de PSD (résumés dans l’encadré 2)31.
Encadré 2: Analyses de laboratoire de dépistage à haut rendement pour la polyneuropathie symétrique distale
Quelle est l’approche au traitement des symptômes de la neuropathie douloureuse?
En général, le traitement de la douleur neuropathique chronique ne dépend pas de sa cause, puisqu’on dispose de peu de données pour orienter le choix de médicaments spécifiquement plus efficaces pour l’une ou l’autre des affections32. Parmi les exceptions notables, mentionnons la névralgie du trijumeau et la douleur neuropathique liée au cancer. Le Groupe d’intérêt spécial sur la douleur neuropathique a publié une ligne directrice internationale sur le traitement pharmacologique de la douleur neuropathique32. En France, une ligne directrice exhaustive plus récente formule des recommandations sur le traitement pharmacologique et non pharmacologique de la douleur neuropathique focale, centrale ou périphérique diffuse33.
Une bonne part de la documentation sur le traitement des symptômes de la neuropathie douloureuse concerne la PDD. La douleur neuropathique est parmi les symptômes les plus invalidants34. Elle s’observe dans environ 40 %–60 % des cas de diabète compliqués de neuropathie, or, peu de malades reçoivent des traitements pour la douleur, même si certains sont reconnus efficaces35,36.
Les lignes directrices en matière de pratique clinique de l’AAN sur le traitement des symptômes de la PDD proviennent d’une méta-analyse qui n’incluait que des essais randomisés et contrôlés dont le traitement actif avait une durée maximum de 16 semaines37. La plupart des essais cliniques ont établi qu’un traitement efficace donnait lieu à une réduction de 30 % de la douleur37 et peu de cas ont obtenu une réduction de plus de 50 %, indépendamment des médicaments utilisés38. Il faut donc informer les malades que l’objectif du traitement est de réduire et non pas d’éliminer la douleur, afin que les attentes soient réalistes quant à l’efficacité des interventions38. Les données de cette méta-analyse ont montré que 4 classes de médicaments oraux réduisent la douleur, soit les antidépresseurs tricycliques, les inhibiteurs de la recapture de la sérotonine et de la noradrénaline (IRSN), les anticalciques et les gabapentinoïdes. L’ampleur des effets a été similaire entre les 4 classes d’agents; et elles sont toutes indiquées comme monothérapies de première intention pour la PDD37. Étant donné l’efficacité similaire des agents, les médecins devraient tenir compte de leur profil d’effets indésirables et de leur coût, de même que des comorbidités des malades avant de choisir l’agent oral de première intention à prescrire.
Les opioïdes peuvent soulager la douleur à court terme de la PDD, mais les données probantes sur leur efficacité à long terme laissent à désirer39,40. Les opioïdes et les opioïdes associés aux IRSN sont déconseillés pour la prise en charge à long terme en raison d’un manque d’efficacité, d’un risque élevé de dépendance et du risque de graves effets indésirables liés à la dose27,37,38. Les médicaments à base de cannabis, comme le nabilone, un cannabinoïde synthétique, peuvent aider à soulager la douleur neuropathique; toutefois, il faudra procéder à d’autres études puisque leurs bienfaits pourraient être contrebalancés par leurs inconvénients potentiels37,41,42.
Les médecins doivent évaluer l’efficacité du traitement de première intention après ajustement de manière à obtenir une dose efficace pendant 6–12 semaines37,43. OPTION-DM, un essai multicentrique randomisé à double insu a comparé l’efficacité des traitements d’association (amitriptyline avec ajout de prégabaline, prégabaline avec complément d’amitriptyline ou duloxétine additionnée de prégabaline) pour ce qui est du paramètre principal (soulagement de la douleur) et des paramètres secondaires (qualité de vie, humeur et sommeil) dans la PDD. Les traitements d’association administrés après l’absence de réponse à la monothérapie à 6 semaines ont donné lieu à une efficacité similaire pour les paramètres tant primaires que secondaires43. Cet essai fournit les données à l’appui du traitement d’association comme modalité de première intention dans les cas de PDD si la réponse à la monothérapie est sousoptimale. Il est important aussi d’évaluer et de traiter les troubles de l’humeur et du sommeil comorbides et d’envisager des interventions topiques ou non pharmacologiques37.
Conclusion
Le diagnostic et la prise en charge de la polyneuropathie requièrent une approche systématique. La polyneuropathie symétrique distale, le sous-type le plus fréquent, se caractérise par la présence de symptômes neuropathiques et de signes à l’examen physique et aux épreuves électrodiagnostiques. La plupart des causes de PSD sont identifiables après une anamnèse soigneuse et des analyses de laboratoire de dépistage à haut rendement, mais dans certains cas, elle est considérée comme idiopathique. En présence de douleurs neuropathiques diabétiques, il faut offrir des options pharmacologiques en fonction des symptômes, qui soulagent efficacement la douleur, sans toutefois l’éliminer complètement. À l’avenir, la recherche devrait tenter de combler les lacunes de nos connaissances actuelles sur le traitement des symptômes de douleur neuropathique causée par la polyneuropathie (encadré 3).
Encadré 3: Questions sans réponses
En présence de signes et symptômes concordant avec une polyneuropathie symétrique distale dont la cause est connue, faut-il toujours demander une consultation pour examen de la conduction nerveuse et électromyographie afin de confirmer le diagnostic?
À partir de quel seuil procède-t-on à des analyses de laboratoire additionnelles en plus des épreuves de dépistage à haut rendement lorsque les signes et symptômes de polyneuropathie progressent?
Faut-il procéder à une biopsie cutanée en présence de symptômes de neuropathie affectant les petites fibres étant donné son vaste diagnostic différentiel?
Quelles sont les meilleures stratégies de prise en charge de la douleur neuropathique causée par la polyneuropathie?
Remerciements
Les auteurs remercient le patient d’avoir autorisé l’utilisation de ses clichés à des fins éducatives pour cet article.
Footnotes
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Collaborateurs: Ario Mirian, Ziyad Aljohani, Daniel Grushka et Anita Florendo-Cumbermack ont contribué à la conception, à l’acquisition des données et à l’interprétation documentaire. Ario Mirian a rédigé l’ébauche du manuscrit. Tous les auteurs ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/