L’utilisation des biosimilaires peut améliorer la concurrence et réduire le coût des médicaments au Canada, mais leur utilisation reste très faible.
L’infliximab, l’étanercept et l’insuline glargine biosimilaires sont inscrits aux listes des médicaments de toutes les provinces; toutefois, des politiques ont limité leur instauration chez les patients encore jamais traités par agents biologiques (« politiques relatives aux nouvelles ordonnances ») et ont pour une bonne part échoué à favoriser l’adoption des biosimilaires.
Même si elles sont controversées, depuis leur adoption en 2019, les politiques qui rendent obligatoire la substitution des agents biologiques de référence par des biosimilaires pour en assurer la couverture par les régimes provinciaux d’assurance médicaments ont grandement contribué à l’augmentation de l’adoption des biosimilaires.
Le marché des biosimilaires au Canada pourrait être consolidé par l’harmonisation des politiques, l’enseignement aux patients et aux prescripteurs et la collaboration avec les fabricants.
Les agents biologiques représentent un segment important des dépenses en médicaments au Canada : alors qu’ils ne constituaient que 1,5 % du volume des ordonnances, les agents biologiques ont généré 27,3 % des dépenses en 20181. En date de 2018, le prix des agents biologiques au Canada, y compris les dépenses par personne, n’arrivait qu’au second rang après les États-Unis parmi les pays de l’Organisation de coopération et de développement économiques (OCDE)2. Par exemple, le Canada a consacré plus d’argent aux anti-TNF (facteur de nécrose tumorale), une classe d’agents biologiques, qu’à tout autre médicament remboursé par les régimes publics3. Au cours des 10 dernières années, le Canada a triplé ses dépenses en agents biologiques et le phénomène ne semble pas en voie de s’estomper4.
Avec plus de 1000 agents biologiques commercialisés au Canada et le fait qu’ils sont utilisés dans la plupart des spécialités cliniques, il devient absolument nécessaire de chercher à en maîtriser les coûts5. Les biosimilaires, des agents dotés d’une efficacité et d’une innocuité semblables à celles des médicaments d’origine, constituent une importante piste de solution1,4,6,7. Or, pour l’instant, seulement 31 biosimilaires sont approuvés au Canada, soit moins de la moitié par rapport au nombre disponible sur le territoire de l’Union européenne, et l’utilisation des biosimilaires au Canada est relativement faible5,8.
Nous avons voulu faire le point sur les politiques actuelles relatives aux biosimilaires et leur utilisation au Canada à l’aide de 3 cas éloquents : l’infliximab, l’étanercept et l’insuline glargine. Nous abordons brièvement l’interchangeabilité et l’extrapolation des indications avant de formuler des suggestions pour améliorer le marché en harmonisant les politiques relatives aux biosimilaires, en favorisant l’enseignement aux patients et aux prescripteurs et en suscitant l’implication des fabricants.
Où en sont les politiques relatives aux biosimilaires au Canada?
Même si plus de 30 biosimilaires ont été approuvés au Canada, leur adoption se fait beaucoup plus lentement que celle des agents génériques classiques1,9. Le cadre actuel des politiques canadiennes relatives à certains des premiers biosimilaires offerts (c.-à-d., infliximab, étanercept et insuline glargine) constitue un important point de départ pour comprendre le marché où ils évoluent.
Infliximab et étanercept biosimilaires
La première version de l’agent anti-TNF infliximab a fait son entrée sur le marché canadien en 2001, suivie en 2014, du premier infliximab biosimilaire approuvé (Inflectra)5. En date de septembre 2015, le Programme commun d’évaluation des médicaments (PCEM) de l’Agence canadienne des médicaments et des technologies de la santé (ACMTS) a publié un rapport favorable sur Inflectra afin qu’il soit inscrit avec les mêmes critères que le médicament d’origine10. Peu de temps après, la Colombie-Britannique et l’Ontario ont inscrit l’infliximab biosimilaire à leurs listes de médicaments pour les personnes encore jamais traitées par infliximab (« politiques relatives aux nouvelles ordonnances »; tableau 1).
Dates d’inscription des biosimilaires aux listes de médicaments et dates de substitution obligatoire (selon le cas) pour l’infliximab, l’étanercept et l’insuline glargine biosimilaires dans les provinces concernées
Deux produits biosimilaires d’un autre agent anti-TNF, l’étanercept, ont été approuvés en 2016 (Brenzys) et 2017 (Erelzi)5. Comme pour l’infliximab, le rapport de l’ACMTS a appuyé Erelzi pour les patients chez qui l’étanercept était jugé nécessaire selon des critères de remboursement comparables à ceux du produit d’origine10. En vertu des politiques sur les nouvelles ordonnances, l’étanercept biosimilaire a été intégré aux listes provinciales de médicaments à partir de juillet 2017 en Colombie-Britannique et à l’Île-du-Prince-Édouard. C’est seulement en 2019 que les provinces canadiennes ont commencé à appliquer des politiques exigeant que les patients déjà sous traitement passent à des agents biosimilaires pour continuer de couvrir l’agent par l’entremise des régimes d’assurance médicaments publics.
Insuline glargine biosimilaire
L’insuline glargine à longue action a été approuvée en 2002, et en 2015, on autorisait la mise en marché d’un biosimilaire5. La même année, l’insuline glargine biosimilaire a reçu l’aval du PCEM, et 2 ans plus tard, elle se retrouvait sur toutes les listes provinciales de médicaments (tableau 1)10. Comme avec l’infliximab et l’étanercept biosimilaires, l’obligation à l’échelle des provinces de passer au nouveau type d’agent n’est entrée en vigueur qu’en 2019.
Comment l’adoption des biosimilaires a-t-elle varié d’une province à l’autre?
À l’heure actuelle, l’infliximab, l’étanercept et l’insuline glargine biosimilaires sont inscrits aux listes de médicaments de toutes les provinces. Des politiques rendant obligatoire la substitution de l’agent biologique d’origine par son biosimilaire pour maintenir sa couverture par le régime public ont été annoncées dans 5 provinces, même si seules la Colombie-Britannique et l’Alberta ont commencé à les appliquer en décembre 2020 (tableau 1). Plusieurs autres provinces et certains assureurs privés ont mis de l’avant des politiques sur les nouvelles ordonnances. Pour explorer l’adoption des biosimilaires, nous avons utilisé les données nationales de l’audit des achats des hôpitaux et des pharmacies du Canada d’IQVIA pour toutes les provinces, à l’exception de Terre-Neuve-et-Labrador, allant de 2017 jusqu’à la fin de 2020.
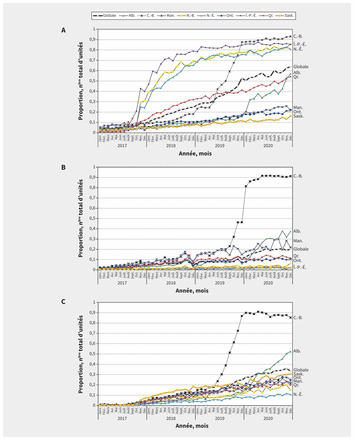
L’adoption des biosimilaires a augmenté avec le temps, même si elle varie substantiellement selon les biosimilaires et les régions (figure 1). Cette hétérogénéité résulte en partie de la couverture inégale offerte par le régime public au Canada. Une fois les agents inscrits, leur adoption peut dépendre de la disponibilité des produits de substitution et de leur statut à l’égard du remboursement (complet ou restreint).
Proportion des unités totales (A) d’insuline glargine, (B) d’infliximab et (C) d’étanercept biosimilaires achetés entre 2017 et la fin de 2020 dans les pharmacies en Alberta (Alb.), en Colombie-Britannique (C.-B.), au Manitoba (Man.), au Nouveau-Brunswick (N.-B.), en Nouvelle-Écosse (N.-É.), en Ontario (Ont.), à l’Île-du-Prince-Édouard (Î.-P.-É.), au Québec (Qc) et en Saskatchewan (Sask.) et données sur l’utilisation globale fournies par l’audit des achats des hôpitaux et des pharmacies du Canada d’IQVIA.
L’exemple le plus frappant de la façon dont la politique peut influencer l’adoption des biosimilaires s’observe peut-être en Colombie-Britannique. Entre mai et novembre 2019, les patients sous insuline glargine ou infliximab et étanercept pour certaines maladies inflammatoires devaient obligatoirement passer au biosimilaire pour bénéficier de l’assurance médicaments provinciale. À la fin de la période d’introduction graduelle, l’adoption des biosimilaires concernés était d’environ 90 %. En décembre 2019, l’Alberta a commencé à appliquer une politique de substitution comparable. Les premières répercussions de cette nouvelle politique sont déjà perceptibles pour l’infliximab, l’étanercept et l’insuline glargine biosimilaires. En revanche, au Manitoba, en Ontario et en Saskatchewan, qui n’ont inscrit l’infliximab et l’étanercept biosimilaires sur leur liste que pour les nouvelles ordonnances, l’adoption n’a pas été aussi marquée (tableau 1 et figure 1).
Les ventes d’insuline glargine sont une autre preuve que le simple fait d’ajouter des biosimilaires aux listes de médicaments provinciales ne garantit pas leur pénétration du marché. Par exemple, le Nouveau-Brunswick, la Nouvelle-Écosse et l’Île-du-Prince-Édouard ont ajouté l’insuline glargine pour une couverture entière à l’automne 2017 et en même temps, ces provinces ont ajouté un critère d’autorisation spéciale pour l’accès au médicament d’origine. Le résultat a été une augmentation marquée des achats d’insuline glargine biosimilaire dans les pharmacies. En revanche, la Saskatchewan et l’Ontario ont introduit une insuline glargine biosimilaire entièrement couverte à peu près à la même période sans restriction de l’accès au produit d’origine; comme l’illustre la figure 1, il n’y a eu aucune augmentation perceptible de l’adoption du biosimilaire dans ces provinces.
À propos d’interchangeabilité et d’extrapolation des indications
Au Canada, lorsque la mise en marché d’un médicament générique est approuvée, il est d’emblée considéré comme interchangeable avec le produit d’origine. Cela est important, car un médicament jugé interchangeable signifie qu’un pharmacien peut servir le générique à la place du produit d’origine sans consulter le prescripteur, à moins que ce dernier n’ait spécifié « ne pas substituer »7.De plus, les régimes payeurs peuvent obliger les pharmaciens à servir un agent générique plutôt qu’un produit d’origine ou le patient doit payer la différence entre le prix des deux agents. Remplacer un produit d’origine part un générique à la pharmacie est un mécanisme qui fait augmenter l’adoption des génériques et leur part de marché. Les médicaments génériques sont bien reçus au Canada : avec une part de marché globale des génériques de 76 % en 2018, ils se classent au troisième rang parmi les pays de l’OCDE en ce qui a trait à l’adoption9.
Contrairement aux génériques, les biosimilaires ne peuvent pas remplacer l’agent de référence dès leur approbation par Santé Canada et, par conséquent, les pharmaciens ne peuvent pas servir un biosimilaire à la place d’un produit d’origine sans l’accord du prescripteur. Il revient plutôt aux gouvernements des provinces et des territoires de décider s’ils instaurent des politiques pour encourager l’adoption des biosimilaires chez les patients qui commencent un traitement biologique ou chez ceux qui prennent déjà un produit d’origine7. Toutefois, le simple fait d’inscrire un biosimilaire à la liste des médicaments n’entraîne pas le taux d’adoption qu’on attend après l’inscription d’un générique, même lorsque plusieurs stratégies ont été utilisées. Cela pourrait s’expliquer en partie par la réticence des médecins et des patients à utiliser des biosimilaires dans le contexte d’une extrapolation des indications11.
L’extrapolation des indications, par laquelle la similarité peut être jugée applicable à d’autres indications sans qu’on ait à mener d’autres essais cliniques, a été un enjeu particulièrement chargé pour les médecins et les patients12,13. Par exemple, parmi les biosimilaires mentionnés, les résultats d’études sur l’infliximab et l’étanercept d’origine qui regroupaient des patients atteints de polyarthrite rhumatoïde ont été utilisés comme données probantes pour d’autres indications (p. ex., Renflexis a été jugé suffisamment comparable à Remicade pour le traitement de la spondylite ankylosante)10. Les craintes entourant l’utilisation de données d’essais cliniques concernant une indication pour appuyer l’utilisation d’un biosimilaire pour une autre indication expliqueraient en partie pourquoi l’adoption varie entre les agents biosimilaires comme l’infliximab et l’étanercept d’une part et l’insuline glargine d’autre part.
Lorsque les biosimilaires ne sont pas considérés comme interchangeables ou qu’ils n’ont pas d’indications additionnelles indirectes, le recours aux politiques de substitution soulève la controverse. Un énoncé de position conjoint de l’Association canadienne de gastroentérologie et de Crohn et Colite Canada appuie l’utilisation de l’infliximab biosimilaire chez les patients encore jamais traités, mais s’est exprimé contre la substitution des agents d’origine en cours chez les patients dont l’état est stable14. En revanche, la Société canadienne de rhumatologie et l’Association canadienne de spondylarthrite appuient généralement la substitution par des biosimilaires sur la base d’un consentement éclairé et moyennant la possibilité de revenir à l’agent biologique d’origine15,16. Les médecins et les patients ont aussi dit craindre les répercussions sur la santé mentale en cas de rechute de la maladie et si l’innocuité et l’efficacité des biosimilaires sont remises en question13,17,18. Au moins un fabricant d’un produit d’origine a fourni une assistance financière aux patients qui commencent leur traitement afin qu’ils obtiennent le produit d’origine pour faire face à la concurrence des biosimilaires19. Il importe de rappeler que la substitution ne fait pas l’unanimité, que des préoccupations sont exprimées à son sujet et qu’elle a des répercussions réelles sur l’indépendance d’esprit des patients et des professionnels de la santé.
Toutefois, si l’adoption des biosimilaires demeure faible, les fabricants pourraient ne pas vouloir prendre les risques associés à leur lancement sur le marché canadien. Cela pourrait avoir des effets négatifs durables tant sur le coût des agents biologiques que sur leur accessibilité à long terme. En effet, avec seulement la moitié du nombre de biosimilaires approuvés par rapport à l’Union européenne, le Canada est peut-être déjà victime de tels effets.
Comment améliorer l’adoption des biosimilaires au Canada?
Au Canada, l’adoption des biosimilaires fait piètre figure (avec environ 1,9 % des 7,7 milliards de dollars consacrés aux agents biologiques en 2018)1. Pour améliorer le marché des biosimilaires, les responsables des orientations politiques des provinces et des territoires devraient envisager de travailler ensemble en vue d’élaborer et adopter des politiques communes, de sensibiliser et soutenir les patients et les professionnels de la santé et de collaborer avec l’industrie.
Harmonisation des politiques
À l’heure actuelle, au Canada, les politiques sur les biosimilaires forment une sorte de macédoine : plusieurs régimes publics (et privés) excluent certains biosimilaires; il y en a qui les rendent obligatoires uniquement pour les nouvelles ordonnances et d’autres exigent d’y recourir d’emblée. Les provinces et les territoires devraient harmoniser l’inscription et le remboursement des biosimilaires. Les politiques qui n’obligent que les nouveaux utilisateurs à prendre un biosimilaire ne semblent pas avoir favorisé efficacement leur utilisation à l’échelle nationale. C’est la substitution obligatoire qui a mené à l’augmentation la plus marquée de l’adoption; mais toute politique qui rend la substitution obligatoire chez les patients sous traitement stable devrait miser sur la sensibilisation des professionnels de la santé et des patients et les soutenir, en plus d’autoriser l’accès au produit d’origine lorsque cela est médicalement justifié.
Soutien aux patients et aux professionnels de la santé
Des doutes légitimes persistent quant à l’innocuité et l’efficacité des biosimilaires chez les patients et les professionnels de la santé. Une revue documentaire systématique sur les croyances des professionnels de la santé a révélé qu’en général, les médecins sont réticents à prescrire des biosimilaires, car ils doutent de leur innocuité, de leur efficacité, et de l’extrapolabilité de leurs indications14. Les études incluses dans cette revue évoquaient un manque de connaissances sur les biosimilaires et concluaient que la prescription des biosimilaires allait être favorisée par le temps et l’expérience acquise avec ces agents. Des données plus récentes provenant d’un groupe de discussion regroupant des régimes payeurs et des professionnels de la santé ont également proposé une meilleure sensibilisation aux biosimilaires comme moyen de promouvoir leur utilisation20. Les programmes de soutien aux patients offerts et généralement défrayés par les fabricants de certains agents biologiques, incluant l’enseignement, la livraison à domicile et des services de soins infirmiers, sont une valeur ajoutée pour les traitements biologiques5.
Participation des fabricants
Avec environ deux fois moins de biosimilaires approuvés comparativement à l’Union européenne, l’amélioration de leur adoption au Canada pourrait inciter d’autres fabricants à accepter les risques associés à tout lancement sur le marché. En retour, une concurrence accrue entre les biosimilaires devrait en théorie donner plus de pouvoir d’achat aux régimes publics et privés et contribuer à une baisse de prix. Il ne faut toutefois pas uniquement miser sur le coût direct parce que les services à valeur ajoutée, comme les soins infirmiers et autres formes de soutien aux patients, sont des aspects importants qui augmentent la valeur totale des agents biologiques6.
Conclusion
Il ne suffit pas qu’un biosimilaire fasse son entrée sur le marché pour en assurer un taux d’utilisation élevé. Les effets des politiques sur les nouvelles ordonnances sont mitigés, tandis que les substitutions obligatoires ont mené à d’importantes augmentations de l’adoption des biosimilaires. Toutefois, plusieurs politiques de substitution ont été introduites après notre période d’analyse et on ignore quelles en sont les répercussions à long terme. Des préoccupations notables persistent chez les patients et les professionnels de la santé, et les responsables des orientations politiques devraient user de prudence, car une évaluation plus approfondie s’impose. Avec une meilleure accessibilité, une saine concurrence et des économies en vue, le temps est venu de surmonter les obstacles à l’adoption des biosimilaires.
Footnotes
Intérêts concurrents: Michael Law a reçu des honoraires de consultant de Santé Canada, du Syndicat des employés d’hôpitaux et du Conference Board du Canada. Il a agi à titre de témoin expert pour le Procureur général du Canada et la Fédération des enseignants de niveau post-secondaire de la Colombie-Britannique. Mina Tadrous a reçu des honoraires de consultante pour l’Agence canadienne des médicaments et des technologies de la santé et la société Green Shield Canada. Tara Gomes est membre du Comité consultatif sur les médicaments et les approches thérapeutiques du ministère Services aux Autochtones Canada. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Collaborateurs: Mina Tadrous a acquis les données d’IQVIA. Alison McClean a rédigé l’ébauche du travail. Tous les auteurs ont substantiellement contribué à la modélisation du travail, y compris à la révision critique du contenu intellectuel important; ils ont approuvé la version finale pour publication et se portent garants du travail.
Financement: Cette recherche a été financée par les Instituts de recherche en santé du Canada (IRSC) par l’entremise d’une subvention de projet (451221), et par une subvention de recherche 2020 de CIORA (Canadian Initiative for Outcomes in Rheumatology cAre) (2020-001). Michael Law a reçu une bourse salariale de la Chaire de recherche du Canada sur l’accès aux médicaments. Tara Gomes a reçu une bourse salariale de la Chaire de recherche du Canada sur la recherche et l’évaluation des politiques en matière de drogues et une subvention du ministère de la Santé de l’Ontario. Mark Harrison a reçu une bourse salariale de la Fondation Michael Smith pour la recherche en santé (16813). Mina Tadrous a reçu des subventions du ministère de la Santé de l’Ontario et des IRSC. Alison McClean a reçu un soutien du programme de bourses d’études supérieures du Canada – niveau maîtrise. IQVIA a fourni les données comme contribution en nature. Les énoncés, observations, conclusions, vues et opinions exprimés dans ce rapport se fondent en partie sur les données obtenues en vertu d’une licence d’IQVIA Solutions Canada inc. concernant les services d’informations suivants : base de données de l’audit des achats des hôpitaux et des pharmacies du Canada, de janvier 2001 à décembre 2020. Tous droits réservés.
Avis: Les énoncés, observations, conclusions, vues et opinions exprimés aux présentes ne reflètent pas nécessairement ceux d’IQVIA inc. ou de ses filiales. Les organismes subventionnaires n’ont joué aucun rôle dans la conception de l’étude, la collecte, l’analyse et l’interprétation des données ou la décision de la publier.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/