Le virus varicelle-zona (VZV) est présent partout dans le monde et il est très infectieux; il se propage par les aérosols ou par contact direct.
La primo-infection par le virus de la varicelle chez l’adulte est associée à un taux élevé de morbidité et de mortalité.
Certains pays ne disposent pas de programmes systémiques de vaccination contre la varicelle; par conséquent, les personnes originaires de ces pays sont exposées à un risque d’infection.
Les lésions cutanées de la varicelle sont parfois négligées chez une personne dont la peau est foncée.
L’examen des dossiers de vaccination, y compris les rappels, est un élément important pour la santé de la population immigrante et pour la prévention de la maladie chez les personnes nées à l’extérieur du Canada.
Patient A
Un homme de 50 ans a consulté au service des urgences après 3 jours d’une intense douleur aiguë à la poitrine avec irradiation au dos, fièvre subjective et inappétence. Il souffrait de diabète, d’hypertension et de dyslipidémie pour lesquels il prenait metformine–sitagliptine, gliclazide, empagliflozine, périndopril–indapamide et rosuvastatine. Il avait aussi pris du méthotrexate pendant plus de 5 ans pour traiter une dermatite atopique. À l’examen, il était afébrile, sa saturation en oxygène était à 98 % à l’air ambiant et il présentait une éruption cutanée papuleuse au tronc et aux membres. Il a été hospitalisé pour examens plus approfondis et prise en charge.
Les analyses de laboratoire sont présentées au tableau 1. La tomodensitométrie (TDM) thoracique, abdominale et pelvienne initiale s’est révélée sans particularités. Nous avons effectué des prélèvements sanguins pour hémocultures lors de l’admission hospitalière; elles ont révélé la présence d’un staphylocoque doré sensible à la méthicilline (MSSA, pour methicillin-susceptible Staphylococcus aureus). Nous avons commencé à lui administrer de la cloxacilline par voie intraveineuse, après quoi les hémocultures ont été négatives. L’échocardiogramme transthoracique n’a révélé aucun signe d’endocardite. Selon l’équipe d’hématologie, sa thrombocytopénie était causée par la bactériémie à MSSA. Le patient ne présentait aucune caractéristique de microangiopathie thrombotique, les résultats des tests pour le VIH, l’hépatite (A, B et C), le cytomégalovirus et le virus d’Epstein–Barr sont restés négatifs.
Sommaire des analyses de laboratoire à l’admission hospitalière
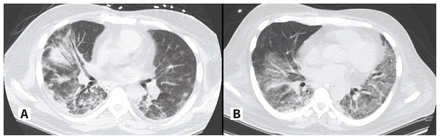
Deux jours après l’hospitalisation, le patient a présenté une insuffisance respiratoire hypoxémique avec choc septique et a été transféré à l’unité des soins intensifs (USI) pour y recevoir des amines vasopressives et une ventilation artificielle. La reprise de la TDM thoracique a montré une consolidation confluente multifocale péribronchique périphérique et des opacités en verre dépoli au poumon droit, de même que des opacités en verre dépoli et des nodules au poumon gauche (figure 1A). Nous avons diagnostiqué une pneumonie extrahospitalière avec choc septique et commencé un traitement par méropénème. Son séjour à l’USI a été compliqué par une pneumonie associée à l’utilisation du respirateur, une insuffisance rénale aiguë et une réaction à la cloxacilline avec éosinophilie et symptômes systémiques. Malgré une antibiothérapie appropriée et un soutien des fonctions vitales, le patient est demeuré dépendant du respirateur. Deux semaines après son admission à l’USI, son frère a été également admis à l’USI pour une situation similaire (figure 2).
Tomodensitométrie thoracique chez (A) un homme de 50 ans (patient A) et (B) un homme de 52 ans (patient B), montrant des infiltrats bilatéraux liés à une primo-infection par le virus de la varicelle.
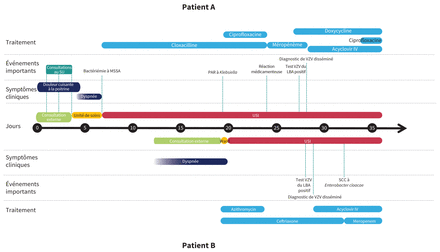
Fil des événements chez un homme de 50 ans (patient A) et un homme de 52 ans (patient B) présentant une primo-infection par le virus de la varicelle. Le Jour 0 correspond à la date d’apparition des premiers symptômes chez le patient A. Remarque: IV = intraveineux, LBA = lavage bronchoalvéolaire, MSSA = Staphylococcus aureus sensible à la méthicilline, PAR = pneumonie associée au respirateur, SCC = septicémie liée au cathéter central, SU = service des urgences, USI = unité des soins intensifs, VZV = virus varicelle-zona.
Patient B
Un homme de 52 ans a consulté au service des urgences pour une dyspnée progressive depuis 1 semaine. Il avait des antécédents de diabète avec néphropathie associée, hypertension et dyslipidémie pour lesquels il prenait metformine, linagliptine, gliclazide, amlodipine–périndopril et rosuvastatine.
En moins de 24 heures, nous avons admis le patient à l’USI pour une insuffisance respiratoire hypoxémique aiguë. Les analyses de laboratoire sont présentées au tableau 1. Une TDM thoracique a montré des opacités multifocales en verre dépoli avec des zones d’épaississement septales intralobulaires indicatrices d’une infection (figure 1B). Nous avons diagnostiqué une pneumonie extrahospitalière.
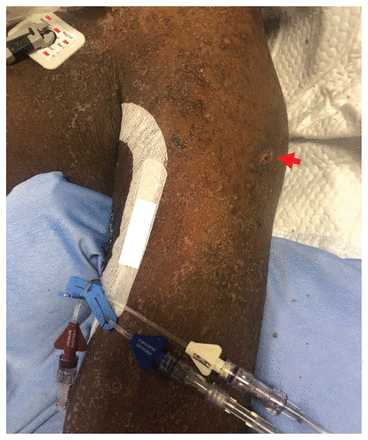
Nous avons procédé à un lavage bronchoalvéolaire chez les 2 patients. Dans les 2 cas, les spécimens analysés par amplification en chaîne par polymérase (ACP) étaient positifs à l’égard du virus varicelle–zona (VZV, pour varicella zoster virus), alors que le bilan viral respiratoire était négatif (virus de la grippe A et B, virus syncytial respiratoire, SRAS-CoV-2). Après ces résultats, nous avons attentivement réexaminé les 2 patients et observé dans les 2 cas des érosions recouvertes de croûtes au visage, au tronc et aux membres supérieurs (figure 3). Les 2 patients ont eu des résultats positifs au dépistage du VZV par ACP sur des échantillons sanguins et des frottis des lésions. Les épreuves sérologiques menées sur les échantillons sanguins prélevés chez les 2 patients lors de l’admission hospitalière, comparativement aux prélèvements effectués plus tard durant leur hospitalisation, ont montré une séroconversion aiguë avec présence d’immunoglobulines G (IgG) anti-VZV.
Photographie d’une érosion recouverte d’une croûte (flèche) au bras gauche d’un homme de 50 ans (patient A), causée par une primoinfection par le virus de la varicelle. On voit sur la peau en arrière-plan plusieurs plaques brunes écailleuses qui desquament, dues à une réaction médicamenteuse avec éosinophilie et symptômes systémiques, et à sa dermatite chronique sous-jacente.
Nous avons diagnostiqué une primo-infection à VZV avec maladie disséminée et pneumonie chez les 2 patients, 28 jours après l’admission hospitalière du patient A et 9 jours après celle du patient B. Nous avons commencé chez les 2 patients de l’acyclovir par voie intraveineuse. Des personnes interrogées ont révélé que les 2 frères vivaient ensemble, avaient immigré au Canada des îles Fidji une vingtaine d’années auparavant et n’avaient pas voyagé récemment. Ils n’avaient jamais reçu de diagnostic de varicelle et n’avaient pas été vaccinés contre la maladie.
Nous avons continué l’acyclovir intraveineux pendant 4 semaines jusqu’à ce que les symptômes s’améliorent et que les lésions se soient asséchées. Nous avons donné son congé au patient A après 61 jours, le patient B est décédé 119 jours après son admission hospitalière des complications d’une septicémie découlant d’une pneumonie hospitalière.
Discussion
L’infection au VZV, connue sous le nom de varicelle, est causée par un virus présent partout dans le monde1,2. Il est extrêmement contagieux et se propage par contact direct avec des lésions ou par inhalation d’aérosols provenant de lésions vésiculaires ou de sécrétions respiratoires infectées1. Depuis l’adoption d’un programme de vaccination publique efficace contre la varicelle au Canada, les taux d’infection au VZV, d’hospitalisations et de décès ont diminué dans toutes les catégories d’âge3. Toutefois, l’âge de la primo-infection est devenu plus tardif en raison de l’immunité collective3. Les adultes nés à l’extérieur du Canada pourraient être particulièrement sensibles à l’absence de programmes systémiques de vaccination anti-VZV ou aux modes de transmission différents dans leur pays d’origine3.
Tableau clinique, diagnostic et prise en charge
L’éventail des manifestations cliniques varie selon l’âge et le statut immunitaire des malades1,2. La primo-infection à VZV durant l’enfance est en général relativement bénigne et autorésolutive chez les enfants en santé1,2. En effet, chez les enfants, la varicelle se manifeste souvent par une légère fièvre et des signes généraux qui rentrent habituellement dans l’ordre quelques jours après le déclenchement d’une éruption maculopapuleuse généralisée.
En revanche, chez les adultes, la primo-infection à VZV est souvent associée à un taux élevé de morbidité et de mortalité2–4. Les complications sont plus fréquentes à l’adolescence et à l’âge adulte, chez les personnes enceintes et les personnes immunodéprimées, que chez les enfants. Elles incluent bactériémie secondaire à des infections de la peau et des tissus mous, pneumonie, hépatite et encéphalite1,2,4,5. Le taux de létalité est le plus élevé chez les adultes4,6.
L’une des complications les plus graves de la maladie disséminée pouvant menacer le pronostic vital est la pneumonie varicelleuse qui s’observe dans 1 cas sur 400 chez les adultes immunocompétents et est associée à une mortalité globale de 10 %–30 %7. Des symptômes respiratoires, incluant dyspnée, toux et tachypnée, apparaissent au cours des 6 premiers jours de la maladie avec de la fièvre1,7. L’imagerie thoracique montre souvent des signes bilatéraux de pneumonie nodulaire ou interstitielle7. Les malades dont l’insuffisance respiratoire s’aggrave et qui ont besoin de ventilation artificielle présentent un taux de mortalité de 43%–50 % malgré l’application de mesures intensives de soutien des fonctions vitales8.
Un diagnostic d’infection à VZV peut être posé sur une base clinique à partir des lésions vésiculaires caractéristiques, à tous les stades du processus infectieux9. La présence du VZV est confirmée par des analyses de laboratoire, notamment des tests ACP sur des frottis des lésions vésiculaires9. La maladie disséminée et les complications sont souvent diagnostiquées par confirmation microbiologique des lésions cutanées au dépistage du VZV par ACP, en plus d’un syndrome clinique compatible, comme la pneumonie ou l’encéphalite. Le liquide céphalorachidien, le sérum et le liquide de lavage bronchique peuvent aussi être soumis à des tests9. La confirmation sérologique d’une infection aiguë est constatée en présence d’IgG anti-VZV9.
L’acyclovir et ses analogues (valacyclovir, famciclovir) sont des antiviraux hautement efficaces pour la primo-infection par le virus de la varicelle. La décision d’utiliser un antiviral dépend de la gravité de l’infection et de facteurs liés à l’hôte1,7. Chez les adultes immunocompétents, les antiviraux ont une période limitée durant laquelle ils peuvent influer sur l’issue de l’infection à VZV, car la majeure partie de la réplication virale cesse 72 heures après l’apparition de l’éruption. En revanche, cette fenêtre temporelle est plus longue chez les hôtes immunodéprimés étant donné que la sécrétion virale se prolonge parfois chez eux. Chez les malades qui présentent des complications graves, notamment une pneumonie varicelleuse, les médecins devraient administrer de l’acyclovir (10 mg/kg) par voie intraveineuse toutes les 8 heures pendant 7–10 jours, la durée dépendant de l’évolution clinique1,7. Outre le traitement antiviral, les soins sont surtout des soins de soutien et la ventilation artificielle s’impose en présence d’insuffisance respiratoire7.
Nos 2 patients n’avaient pas d’antécédents de primo-infection par le virus de la varicelle durant l’enfance et avaient immigré à l’âge adulte des îles Fidji, qui n’ont pas de programme de vaccination contre la varicelle. Cela les a rendus sensibles à la primo-infection à VZV à l’âge adulte. Leur séroconversion aiguë, avec IgG anti-VZV et éruption cutanée disséminée (dont l’importance n’a pas été reconnue initialement), concordait avec la primo-infection par le virus de la varicelle qui n’a été diagnostiquée qu’après une certaine période d’hospitalisation. Les 2 frères ont développé des complications de la varicelle, dont une maladie disséminée avec pneumonie varicelleuse et, dans le cas du patient A, une bactériémie des suites d’une infection bactérienne secondaire de la peau et des tissus mous. La vaccination ciblée des adultes qui ont immigré de pays où il n’y a pas d’immunisation contre le VZV pourrait être une stratégie efficace de prévention de la primo-infection et de ses complications3.
Chez les 2 patients, le diagnostic de primo-infection par le virus de la varicelle a été posé après l’analyse du liquide de lavage bronchoalvéolaire par ACP qui a révélé la présence du VZV. Les 2 ont subi un autre examen dermatologique qui a révélé la présence d’érosions et de croûtes, signes de la varicelle. Un facteur qui a probablement contribué au retard du diagnostic est le type de peau 5 à l’Échelle de Fitzpatrick chez les 2 patients. Certains médecins connaissent moins l’examen dermatologique des peaux foncées et une mauvaise interprétation des résultats peut mener à des soins sous-optimaux10,11. La varicelle a de tout temps été décrite par la présence de papules érythémateuses qui se transforment en petites vésicules claires entourées d’un halo érythémateux sur lequel se forment éventuellement des croûtes, mais l’érythème n’est pas aussi clairement perceptible sur une peau plus foncée10,11. Chez les malades dont la peau est foncée, l’érythème n’est pas toujours présent ou peut prendre une teinte violacée11. Les médecins trouveront l’utilisation du bout des doigts pratique pour palper les changements de texture de la peau (p. ex., chez les patients qui souffrent de dermatite atopique)11. Il faut offrir des illustrations cliniques plus variées lors des séances de formation et d’enseignement aux médecins afin de mieux les préparer à diagnostiquer les maladies cutanées chez les malades dont la peau est plus foncée10.
Footnotes
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement des patients.
Collaborateurs: Tous les auteurs ont collaboré à la conception du travail. Jordan Mah, Anthony Lieu, Emma Heck et Alejandra Ugarte-Torres ont rédigé l’ébauche du manuscrit. Tous les auteurs en ont révisé de façon critique le contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/