Une infection aiguë au cytomégalovirus (CMV) peut survenir chez des adultes âgés qui ne sont pas visiblement immunovulnérables et on devrait l’envisager parmi les diagnostics différentiels chez des patients présentant de la fièvre d’origine inconnue.
On devrait répéter la sérologie du CMV si on soupçonne une infection, mais que les résultats initiaux sont négatifs; un test d’amplification en chaîne par polymérase pour le CMV peut aussi être utile.
Chez des patients qui ne sont pas immunovulnérables, une infection aiguë au CMV ne nécessite généralement pas de traitement antiviral.
On a hospitalisé une femme de 61 ans à notre établissement communautaire de taille moyenne situé dans le nord-est du Japon pour un cas de fièvre. Elle se portait bien jusqu’au neuvième jour précédent son hospitalisation lorsqu’une fièvre constante oscillant entre 38 °C et 39 °C s’est manifestée. À sa connaissance, elle n’avait pas eu de contact avec des personnes malades. Elle travaillait comme employée de bureau, avait des antécédents d’asthme et de thyroïdite, ne fumait pas ni ne consommait d’alcool et prenait régulièrement de la bilastine. Elle avait consulté la clinique 8 jours avant son hospitalisation et on lui a prescrit une antibiothérapie administrée sous forme orale (cefditoren pivoxil); son état ne s’est cependant pas amélioré. Un érythème s’est manifesté 7 jours avant son hospitalisation et on l’a orienté 2 jours plus tard vers le service de consultation externe de notre hôpital. À ce moment, l’examen a montré de petites papules érythémateuses sur son abdomen, ses bras et ses jambes. Les analyses de laboratoire ont révélé une numération leucocytaire de 5,10 (plage normale 3,30–8,60) × 109/L, une numération de neutrophiles de 2,17 (plage normale 1,70–6,34) × 109/L, une numération de lymphocytes de 2,23 (plage normale 0,96–3,10) × 109/L et une numération de plaquettes de 172 (plage normale 158–348) × 109/L. Le niveau sérique de protéines C réactives de la patiente atteignait 14,4 (plage normale 0,0–3,0) mg/L, celui de l’aspartate aminotransférase atteignait 35 (plage normale 11–32) U/L et celui de γ-glutamyl transférase atteignait 46 (plage normale 5–35) U/L. On soupçonnait une infection virale, mais on ne lui a pas prescrit de traitement en particulier. À ce moment, on a procédé au dépistage des anticorps du cytomégalovirus (CMV) et du virus d’Epstein–Barr (VEB). Elle a consulté le service des urgences à nouveau, 2 jours avant son hospitalisation, car elle n’arrivait pas à s’alimenter en raison de la fièvre, d’une anorexie et d’un mal de gorge. On n’a pas trouvé la cause de sa fièvre et on a prévu l’hospitaliser pour de plus amples examens. La journée précédant son hospitalisation, son érythème a disparu.
Lors de l’hospitalisation de la patiente, elle était pleinement consciente. Sa tension artérielle était de 122/88 mm Hg, sa fréquence cardiaque atteignait 105 battements/min, sa température corporelle était de 38,0 °C et sa saturation en oxygène atteignait 99 % à l’air ambiant. Sa peau n’était pas pâle ni ictérique; elle ne présentait pas d’hémorragies conjonctivales. L’examen de son oropharynx n’a révélé aucun œdème pharyngé, sans exsudats ou lésions. Son cou était souple. Nous n’avons pas détecté d’anomalies lors de l’examen cardiovasculaire ou de l’auscultation pulmonaire. Son abdomen était plat et mou, sans présence d’hépatosplénomégalie palpable. Elle ne présentait pas de sensibilité spinale ou costovertébrale ni d’éruption cutanée ou d’œdème périphérique.
Les analyses de laboratoire ont révélé une numération leucocytaire légèrement augmentée de 9,40 × 109/L, accompagnée d’une numération de neutrophiles de 5,83 × 109/L et de lymphocytes de 2,91 × 109/L. Sa numération plaquettaire atteignait 202 × 109/L. Les niveaux d’aspartate aminotransférase (54 U/L), d’alanine aminotransférase (51 U/L), de γ-glutamyl transférase (60 [plage normale 5–35] U/L), de protéines C réactives (51,0 mg/L) et de D-dimères (11 800 [référence 0–1000] μg/L) étaient élevés. Le résultat du test de détection d’antigènes pour le SRAS-CoV-2 était négatif. Nous avons détecté un petit nombre de protéines (1+), une légère hématurie microscopique (1+), quelques bactéries, mais aucun leucocyte sur l’analyse d’urine. La radiographie thoracique de la patiente était normale.
Nous avons envisagé une infection virale (dont une mononucléose infectieuse), une infection bactérienne (dont une endocardite infectieuse et la tuberculose), une maladie auto-immune et un cancer (dont un lymphome) comme diagnostics différentiels, sur la base de la fièvre persistante, de la transaminite modérée, de la légère protéinurie et de l’hématurie microscopique. Nous n’avons pas envisagé une toxoplasmose, car la patiente ne présentait pas de facteurs de risque. Un résultat du test de dépistage du VIH s’est avéré négatif. On n’a pas observé la présence d’anticorps cytoplasmiques antinucléaires et antineutrophiles et aucune bactérie ni aucun champignon n’a cru sur les cultures sanguines ou urinaires. En raison de l’ensemble des résultats de son hémogramme, elle ne répondait pas aux critères d’une lymphohistiocytose hémophagocytaire. Nous n’avons pas demandé d’écouvillonnages nasopharyngés dans le cadre de tests antigéniques pour des virus respiratoires, car la patiente n’avait pas mentionné de contacts avec des personnes malades et ne présentait pas de symptômes respiratoires. Un examen tomodensitométrique du thorax et de l’abdomen avec agent de contraste n’a révélé qu’un kyste hépatique et aucun foyer d’infection.
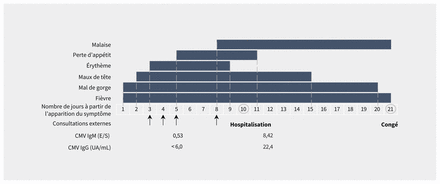
Pendant son séjour à l’hôpital, la fièvre de la patiente a persisté, mais son état général est demeuré stable. Trois jours après le début de son séjour à l’hôpital, on a obtenu les résultats des tests de dépistage des anticorps du CMV et du VEB (réalisés sur des échantillons prélevés 5 jours avant l’hospitalisation) et ils ont révélé une infection antérieure au VEB, mais étaient négatifs à la présence des immunoglobulines M et G (IgM et IgG) du CMV. Comme un résultat négatif à la présence du CMV est faible au Japon pour son groupe d’âge (environ 3 %)1,2, nous avons soupçonné une erreur d’analyse et procédé à nouveau à un test de dépistage de la présence d’anticorps du CMV sérique. Nous n’avons pas demandé un test d’amplification en chaîne par polymérase (PCR) pour diagnostiquer l’infection primaire au CMV, car ce test n’est pas remboursé par le système d’assurance-maladie national. Le sixième jour, les résultats du test de dépistage des IgM et IgG du CMV se sont avérés positifs (figure 1) et nous avons diagnostiqué une infection aiguë au CMV, sans maladie invasive des tissus. En cherchant davantage, la patiente s’est souvenue avoir partagé des ustensiles de cuisine avec une autre personne, une possible voie d’infection. Comme elle n’était pas immunovulnérable, nous n’avons pas administré de traitement antiviral particulier, comme le valganciclovir ou le ganciclovir, qu’on emploie pour traiter la maladie causée par le CMV chez des patients immunovulnérables. Nous avons traité la patiente avec un anti-inflammatoire non stéroïdien et elle a obtenu son congé au 12e jour de son hospitalisation.
Le décours temporel des symptômes et les titres des anticorps pour le cytomégalovirus (CMV). Les valeurs normales pour l’immunoglobuline M (IgM) du CMV: < 0,85; pour l’immunoglobuline G (IgG) du CMV: < 6,0.
Comme la durée moyenne d’une infection symptomatique au CMV est de 8 semaines3, nous avons suivi la patiente sans examen supplémentaire. Sa fièvre et ses malaises se sont complètement résorbés en moins de 4 semaines après l’obtention de son congé hospitalier. Elle se portait bien au dernier rendez-vous de suivi en consultation externe, 3 mois après son congé.
Discussion
L’ampleur de l’infection au CMV peut varier, allant d’une infection asymptomatique à une maladie invasive des tissus. Les cliniciens devraient reconnaître la différence entre une infection au CMV et une maladie causée par le CMV: la première faire référence à l’observation de la réplication du virus, sans égard aux symptômes, alors que la seconde faire référence à l’observation de l’infection au CMV accompagnée des symptômes attribuables au virus. Par ailleurs, la maladie causée par le CMV peut être catégorisée comme un syndrome viral (p. ex., fièvre, malaise, leucopénie, neutropénie, thrombocytopénie, élévation des aminotransférases hépatiques) ou une maladie invasive des tissus4,5. La maladie invasive des tissus est définie par des symptômes cliniques appropriés et des signes d’atteinte aux organes cibles (p. ex., entérite, hépatite, néphrite, pneumopathie, méningo-encéphalite, rétinite) accompagnés de l’observation documentée de la présence du CMV dans les tissus de l’organe atteint4,5. Chez les patients immunocompétents, la plupart des infections sont asymptomatiques et le tableau clinique le plus fréquent est une mononucléose au CMV avec signe de fièvre, de malaise, de maux de gorge, de maux de tête, de lymphocytose, la présence d’au moins 10 % de lymphocytes atypiques et l’élévation des niveaux d’aminotransférases hépatiques6. Bien que la maladie invasive des tissus causée par le CMV peut survenir chez des patients immunocompétents7, sa prévalence est faible. Par contre, pour les patients immunovulnérables (p. ex., ceux qui viennent de subir une transplantation, ont une infection au VIH, reçoivent des traitements immunomodulateurs) et les nourrissons atteints d’une infection congénitale au CMV, la maladie invasive des tissus est une préoccupation importante6.
La séroprévalence du CMV varie selon les régions, tendant à être plus importante en Afrique, en Asie et en Amérique du Sud et moins importante en Europe et en Amérique du Nord8. Une précédente étude a estimé que la séroprévalence mondiale moyenne pour la population générale atteignait 83 %; la séroprévalence du CMV serait de 42 % au Canada et de 72 % au Japon8. Cette séroprévalence du CMV s’accroît avec l’âge et dans les pays où elle est élevée, comme au Japon, la séropositivité atteint presque 100 % chez les personnes de 60 ans et plus1. Au Canada, on a rapporté que 67 %–73 % des donneurs de sang et d’organes ainsi que des receveurs d’organes étaient séropositifs au CMV à l’âge de 70 ans9.
Les approches diagnostiques pour l’infection et la malade au CMV dépendent des antécédents cliniques du patient. Pour diagnostiquer une infection primaire au CMV chez des patients immunocompétents, des études sérologiques sont la norme: soit la détection de l’IgM du CMV ou une élévation du titre des IgG sériques de 4 fois la valeur normale (habituellement mesurées à au moins 2 semaines d’intervalle) confirme le diagnostic. Typiquement, on peut détecter les anticorps IgM du CMV dans les 2 premières semaines et leur valeur peut demeurer élevée pour plusieurs mois ou même jusqu’à une année6,10. Les anticorps IgG du virus sont détectables de 2–3 semaines après l’apparition des symptômes10. Lorsqu’on soupçonne le diagnostic, mais qu’on observe une absence des anticorps IgM et IgG, un test de dépistage sérologique réalisé de 1–2 semaines plus tard peut confirmer la séroconversion. Dans cette situation, un test de dépistage PCR peut s’avérer utile pour le diagnostic en temps opportun d’une infection primaire au CMV. Cependant, comme la sensibilité et la spécificité d’un test PCR peuvent être faibles6,10, l’emploi d’un tel test sans l’appui d’une autre méthode de dépistage n’est pas recommandé pour le diagnostic d’une infection au CMV chez les patients immunocompétents. Par contre, pour les patients immunovulnérables, tout particulièrement ceux qui ont subi une transplantation, le test de dépistage PCR est favorisé et les analyses sérologiques ne jouent aucun rôle dans le dépistage de la forme active de l’infection et de la maladie au CMV. Cela s’explique par le fait que les infections primaires et secondaires causées par la réactivation du CMV chez les patients séropositifs sont fréquentes dans la population de patients4. On favorise aussi le test d’amplification en chaîne par polymérase avec cette population, car une détection et un suivi rapide des niveaux d’ADN sont requis pour sélectionner le traitement antiviral approprié et décider de la durée de la thérapie chez les patients immunovulnérables qui sont atteints de la maladie à CMV. Chez ces patients, la mesure des niveaux de IgG du CMV est utile pour évaluer la présence latente de l’infection au CMV afin de stratifier le risque d’infection et de maladie au CMV.
L’infection et la maladie à CMV chez les patients immunocompétents se résorbent généralement d’elles-mêmes et un traitement antiviral n’est habituellement pas nécessaire; même dans les cas graves de la maladie, l’avantage du traitement antiviral est non concluant7. En revanche, la plupart des patients atteints de l’infection à CMV qui ont subi une transplantation, même s’ils sont asymptomatiques, requièrent un traitement antiviral afin de prévenir le développement d’une maladie invasive des tissus (traitement préventif). En ce qui a trait au traitement préventif, l’administration de valganciclovir sous forme orale est généralement choisie et on traite les patients jusqu’à ce que la charge virale devienne indétectable ou sous la limite de quantification inférieure de l’essai4. Concernant la maladie à CMV symptomatique chez des patients ayant subi une transplantation, l’administration de valganciclovir par voie orale ou de ganciclovir sous forme intraveineuse est recommandée jusqu’à l’éradication de l’ADN du CMV sous la limite de quantification inférieure (< 200 IU/mL) et la résorption de tous les symptômes cliniques de la maladieà CMV4.
La section Études de cas présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs: www.cmaj.ca
Footnotes
Intérêts concurrents: Yukinori Harada déclare avoir reçu une subvention de recherche scientifique de la Société japonaise pour la promotion de la science (KAKENHI) et des honoraires de la société PRECISION Japan Inc., pour les frais de publication. Le Dr Harada déclare aussi être un coreprésentant bénévole du Groupe de travail sur l’excellence du diagnostic de la Société japonaise des hôpitaux de médecine générale. Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement de la patiente.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception du travail. Mai Hongo a rédigé le manuscrit. Tous les auteurs ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/