Un bloc cardiaque chez des patients de moins de 65 ans est rarement causé par une maladie dégénérative du système de conduction.
On devrait entreprendre une évaluation complète des causes secondaires d’un bloc cardiaque avant d’insérer un stimulateur cardiaque de façon permanente.
Les investigations d’une sarcoïdose cardiaque par méthode d’imagerie comprennent une échocardiographie transthoracique, un examen d’imagerie par résonance magnétique cardiaque, une tomodensitométrie thoracique et une tomographie par émission de positrons au fluorodésoxyglucose.
Le traitement de la sarcoïdose cardiaque comprend une immunosuppression à l’aide de prednisone et parfois, de méthotrexate.
Un homme de 60 ans s’est présenté au service des urgences après un bref épisode de syncope sans prodrome. Le patient était alerte et orienté après l’épisode et les témoins n’ont pas rapporté d’activité convulsivante. Il n’avait pas d’antécédents de syncope, mais il présentait des antécédents d’hypertension et de néphrectomie du côté gauche (il était un donneur électif). Son seul médicament était de l’amlodipine prise oralement à une dose de 5 mg/j. Il ne souffrait pas d’allergies et fumait un demipaquet de cigarettes par jour. Il ne consommait pas de cannabis, d’alcool ou de drogues illicites.
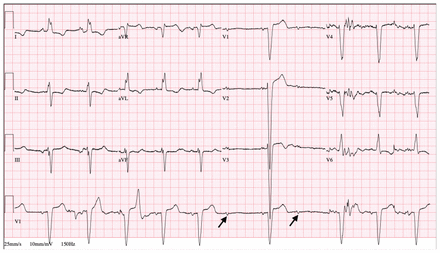
Sa tension artérielle était de 190/80 mm Hg et sa fréquence cardiaque était de 35 à 40 battements/min. Sa température, sa saturation en oxygène et sa fréquence respiratoire étaient normales tout comme le reste de son examen physique. Un électrocardiogramme (ECG) a révélé un bloc auriculo-ventriculaire (BAV) 2:1 accompagné d’un bloc de branche gauche du faisceau (figure 1). Aucun ECG antérieur n’était disponible. La radiographie thoracique était normale. Le patient présentait un hémogramme complet, des électrolytes, une fonction rénale, des enzymes hépatiques et des taux de thyréostimuline normaux, ce qui a exclu des anomalies électrolytiques et une maladie thyroïdienne comme cause du bloc cardiaque. Les dosages ultrasensibles des troponines T étaient un peu élevés (23, 60 et 84 [valeurs de référence de 0 à 14] ng/L). Nous avons hospitalisé le patient afin de poursuivre les investigations, dont une analyse des taux de protéine C réactive, des immunoglobulines, du panel de dosage des vascularites, des hémocultures et du test sérologique de Lyme, et toutes se sont révélées négatives. Ainsi, vous avons considéré qu’il était peu probable que le bloc cardiaque soit causé par des maladies infectieuses ou autoimmunes (encadré 1).
Électrocardiogramme à 12 dérivations chez un homme de 60 ans révélant un bloc auriculo-ventriculaire (flèches). Une télémétrie continue a confirmé un bloc auriculo-ventriculaire de haut grade.
Causes d’un bloc cardiaque chez les adultes
Tonus vagal augmenté
Maladie dégénérative du système de conduction
Ischémique (cardiopathie ischémique, infarctus aigu du myocarde)
Infectieuse (cardite de Lyme, endocardite accompagnée d’un abcès à la racine aortique, rhumatisme articulaire aigu, myocardite d’origine virale)
Métabolique (hyperkaliémie, hypothyroïdie, hyperthyroïdie)
Infiltrante (sarcoïdose, amylose, hémochromatose)
Médicamenteuse (bêtabloquants, inhibiteurs des canaux calciques, antiarythmisants, digoxine)
Iatrogénique (chirurgie cardiaque, remplacement valvulaire aortique par cathéter, ablation par cathéter de certaines arythmies, ablation septale à l’alcool)
Une échocardiographie transthoracique (ETT) a montré une fonction systolique du ventricule gauche modérément diminuée (FEVG 40) accompagnée d’anomalies du mouvement de la paroi dans une distribution non coronaire et une hypertrophie légère du ventricule gauche. Une coronarographie montrait des artères coronaires normales, ce qui éliminait la possibilité d’une coronaropathie. Après son hospitalisation, le patient a subi de multiples épisodes d’étourdissement et de symptômes s’approchant de la syncope avec une fréquence cardiaque chutant dans les 20 battements selon la télémétrie. Nous avons inséré un stimulateur cardiaque veineux temporaire d’urgence.
Malheureusement, le patient continuait à ressentir des symptômes et des épisodes de non-enregistrement de la stimulation cardiaque; nous avons donc implanté un stimulateur cardiaque double-chambre compatible avec l’imagerie par résonance magnétique (IRM) au deuxième jour de son hospitalisation, avant que notre examen pour trouver les causes secondaires au bloc cardiaque ne soit complété.
Une tomodensitométrie (TDM) thoracique du patient a révélé de multiples nœuds lymphoïdes médiastinaux et paratrachéaux d’une taille supérieure à 1 cm, des nodules pulmonaires dispersés, mais aucune adénopathie hilaire, laquelle trahirait la présence d’une sarcoïdose, selon nous. L’examen d’IRM cardiaque a montré un rehaussement tardif après injection de gadolinium de la paroi apicale inférieure et un rehaussement sous-épicardique de la paroi basale antérieure et moyenne septale, suggérant une cardiomyopathie non ischémique (figure 2). Nous n’avons pas effectué de biopsie endomyocardique ventriculaire droite puisque les résultats de l’examen d’IRM n’ont révélé aucun rehaussement tardif après l’injection de gadolinium dans la région habituellement ciblée par la biopsie. Plutôt, nous avons procédé à une biopsie pulmonaire transbronchique qui a démontré la présence d’inflammation granulomateuse non caséeuse, compatible avec une sarcoïdose.
A) Examen d’imagerie par résonance magnétique (IRM) cardiaque montrant un rehaussement tardif sous-épicardique après injection de gadolinium (LGE) de la paroi basale antérieure et moyenne septale (flèches). B) Examen d’IRM cardiaque montrant un rehaussement tardif après injection de gadolinium de la paroi apicale inférieure (sous-endocardique à mi-myocardique) (flèches).
Nous avons amorcé le traitement avec de la prednisone administrée par voie orale à un dosage de 40 mg/j, avec une diminution progressive de 5 mg/s. Nous avons aussi amorcé les traitements médicaux préconisés par les lignes directrices pour les cas d’insuffisance cardiaque accompagnée d’une fraction d’éjection réduite (un antagoniste des récepteurs de l’angiotensine, un bêtabloquant et un antagoniste des récepteurs des minéralocorticoïdes), en raison de la fonction diminuée du ventricule gauche du patient1,2.
On a demandé une tomographie par émission de positrons (TEP) marquée au fluorodésoxyglucose; malheureusement, l’examen s’est tenu 10 mois après l’hospitalisation. Il a révélé une captation intense du traceur sur l’ensemble de la paroi antérolatérale et une captation modérée dans les parois inférieure, antéro-septale et de l’apex (figure 3A). À la lumière de ces résultats, nous avons augmenté la dose de prednisone (passant de 10 mg à 40 mg) et nous avons ajouté le méthotrexate. Nous avons changé le stimulateur cardiaque du patient pour un appareil de resynchronisation cardiaque (TRC) muni d’un défibrillateur cardioverteur implantable, puisque l’examen de son stimulateur cardiaque a dévoilé l’existence d’un dysfonctionnement persistant du ventricule gauche et d’épisodes de fréquences ventriculaires élevées2.
A) Tomographie par émission de positrons (TEP) marquée au fluorodésoxyglucose révélant une captation intense du traceur sur l’ensemble de la paroi antérolatérale (flèches blanches) et une captation modérée de la paroi inférieure, la paroi basale à moyenne antéro-septale et celle de l’apex (flèche noire). B) Examen de suivi en TEP après 6 mois, ne montrant aucune inflammation importante.
Nous avons répété la TEP marquée au fluorodésoxyglucose après 6 mois. Sa fraction d’éjection s’était améliorée (52 %) et aucune inflammation substantielle n’était apparente, comparativement à l’examen TEP précédent (figure 3B). Une reprise de l’ETT a confirmé une fonction du ventricule gauche normale. L’état du patient est maintenant stable, sous médication de prednisone (5 mg) et de méthotrexate (15 mg), administrée par voie orale.
Discussion
Parmi les nombreuses causes des BAV, on compte des formes congénitales et acquises (encadré 1). Les causes dégénératives sont de loin les plus fréquentes et sont associées à des dégénérescences liées à l’âge et à une fibrose du système de conduction, au diabète et à l’hypertension3. Dans le cadre d’une analyse rétrospective, 0,6 % des cas contrôle et jusqu’à 1,1 % des patients hospitalisés (âgés de 65,8 ± 11,3 ans) atteints de diabète présentaient un BAV complet4.
Si l’état de santé du patient est cliniquement stable, on devrait envisager les causes de BAV communes et potentiellement réversibles (qui sont fréquentes chez les patients de moins de 65 ans) et les traiter avant de procéder à l’insertion d’un stimulateur cardiaque permanent. Parmi les causes réversibles, on compte la prise de médicaments, une ischémie, une hyperkaliémie, une dysfonction thyroïdienne ainsi que des infections comme la cardite de Lyme. La maladie de Lyme est une maladie infectieuse à transmission vectorielle dont l’incidence a augmenté dramatiquement dans certaines parties du Canada (144 cas en 2009 contre 2025 cas en 2017)5. Un BAV est présent chez 90 % des patients atteints de cardite de Lyme et il se résorbe à l’aide d’une antibiothérapie dans la plupart des cas5.
La sarcoïdose est une maladie granulomateuse multisystémique de cause inconnue; on peut la reconnaître par des granulomes non caséeux présents dans les prélèvements de biopsie. Elle concerne principalement les personnes dans la trentaine et la quarantaine6. La sarcoïdose touche généralement les femmes, les non-fumeurs, les personnes de descendance africaine et les résidents des latitudes septentrionales6. Dans le cadre d’une étude de cohorte en Ontario, la prévalence de la sarcoïdose a augmenté entre 1996 et 2015, passant de 66 cas à 143 cas par 100 000 habitants7; un accroissement observé à l’échelle mondiale. La sarcoïdose est une grande imitatrice d’autres maladies, complexifiant le diagnostic.
Les poumons et les ganglions du hile sont atteints chez 90 % des patients ayant une sarcoïdose. Cependant, cette maladie peut aussi toucher d’autres organes, dont le cœur, le foie, la peau et les yeux. La sarcoïdose cardiaque (SC) peut être la première manifestation clinique et on l’associe à un pronostic plus sombre en raison d’une insuffisance cardiaque ou d’une mort cardiaque subite8. Dans le cadre d’une étude, 19 % des patients présentant une fraction d’éjection inférieure à 30 % étaient toujours en vie après 10 ans9. On a rapporté une atteinte cardiaque liée à la sarcoïdose dans 27 % des autopsies dans certaines cohortes nordaméricaines, mais de nombreux cas peuvent passer inaperçus10.
Les caractéristiques cliniques de la SC comprennent des anomalies de conduction, comme de la tachycardie ventriculaire et des BAV, de l’insuffisance cardiaque et une mort cardiaque subite, de même que des symptômes non spécifiques comme des douleurs thoraciques, de la fatigue et une présyncope8. L’ampleur, le site et l’étendue de l’inflammation et de la fibrose influencent le tableau clinique. Par exemple, un patient atteint d’une SC localisée dans le nœud auriculo-ventriculaire peut souffrir d’une forme aiguë de bloc cardiaque alors qu’un autre patient atteint d’une SC dont la distribution est fragmentaire peut demeurer asymptomatique, même s’il présente un plus haut risque d’insuffisance cardiaque et d’arythmie ventriculaire.
On procède au diagnostic de cette maladie par analyse histologique, à partir de tissus myocardiques, ou de façon clinique, fondé sur les antécédents du patient ainsi que les résultats d’examens effractifs et non effractifs1. Les biomarqueurs, les ECG et les ETT représentent des analyses de première intention qui mènent souvent à des résultats non spécifiques. Par exemple, une ETT peut montrer des anomalies régionales du mouvement de la paroi dans une distribution non coronaire, avec ou sans dysfonctionnement systolique du ventricule gauche, un amincissement du segment interventriculaire basal et une déformation longitudinale globale réduite. La référence standard demeure la biopsie endomyocardique; cependant, le taux de détection obtenu des biopsies est inférieur à 50 %11. La cartographie électro-anatomique semble prometteuse en augmentant le taux de détection de ces biopsies12. Si un diagnostic tissulaire est impossible, les lignes directrices consensuelles en matière des critères de la Société de rythmologie et le ministère de la Santé et du Bien-être du Japon peuvent être employées8. Les systèmes hybrides d’IRM cardiaque et de TEP au fluorodésoxyglucose détectent l’inflammation et les cicatrices de la SC; ils soulignent ainsi efficacement les différents stades de la SC à l’aide d’une seule modalité d’imagerie13. Idéalement, cet examen devrait être complété 3 mois après avoir amorcé ou interrompu un traitement et si une modification des symptômes se manifeste1,8. Les systèmes d’imagerie hybride TEP et IRM démontrent une plus haute sensibilité et une meilleure précision dans la détection de l’inflammation comparativement aux systèmes TEP et IRM individuels14. Il s’agit d’une nouvelle modalité d’imagerie pour la détection de la SC, qui expose les patients à une dose moindre de rayonnement.
Les données portant sur le dépistage de la SC chez des patients présentant un diagnostic de sarcoïdose sont limitées; cependant, les résultats d’une étude portant sur l’examen des diagnostics et des pronostics de patients suivis en consultation externe suggéraient que si un patient avait des palpitations ou des symptômes de syncope ou de présyncope, un ECG, une électrocardiographie ambulatoire et une ETT devraient être réalisés15. Les résultats anormaux des tests de dépistage et les soupçons cliniques de SC qui perdurent devraient enclencher des examens plus approfondis en IRM, en TEP ou en une version hybride de ces modalités d’imagerie.
La prise en charge de la SC peut être difficile et l’orientation vers un cardiologue possédant une expertise dans le domaine est recommandée1. Une immunosuppression par la prednisone est la pierre angulaire du traitement contre la SC1; on devrait l’envisager lorsque la démonstration de la présence d’inflammation myocardique par des modalités d’imagerie et de la manifestation de BAV, de tachycardie ventriculaire fréquente, soutenue ou non, ou de dysfonctionnement du ventricule gauche8 est réalisée. En plus de l’administration de glucocorticoïdes, des agents non stéroïdiens comme le méthotrexate, l’azathioprine et le mycophénolate devraient être envisagés. En ce moment, l’essai multicentrique randomisé portant sur la SC (CHASM CS-RCT) se poursuit. Dans le cadre de cet essai, les patients atteints de SC sont traités de façon aléatoire à l’aide de prednisone ou de prednisone associée au méthotrexate; l’essai fournira des données probantes utiles pour le traitement de la SC16. Des agents biologiques constituent une thérapie de troisième intention et on n’a rapporté leur utilisation que dans quelques cas. On devrait envisager une thérapie par défibrillateur cardioverteur implantable puisque les patients atteints de sarcoïdose peuvent souffrir d’arythmies ventriculaires.
Pour les patients de moins de 65 ans qui présentent un bloc cardiaque, on devrait aussi envisager la SC avec les autres causes non ischémiques. De nouvelles techniques d’imagerie médicale, comme les systèmes d’imagerie hybrides TEP et IRM, ont augmenté la sensibilité et la précision des diagnostics et les essais cliniques en cours éclaireront davantage la prise en charge.
La section Études de cas présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs : www.cmaj.ca.
Footnotes
Intérêts concurrents : Andrew Moeller déclare recevoir des honoraires de conférencier de la société Novartis et être membre d’un comité consultatif de Novartis (sacubitril-valsartan) et de la société Bayer (vericiguat). Aucun autre intérêt concurrent n’a été déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement du patient.
Collaborateurs: Les deux auteurs ont contribué à l’élaboration et à la conception du travail. Ashar Pirzada a produit l’ébauche du manuscrit. Les deux auteurs ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
Il s’agit d’un article en libre accès distribué conformément aux modalités de la licence Creative Commons Attribution (CC BY-NC-ND 4.0), qui permet l’utilisation, la diffusion et la reproduction de tout médium à la condition que la publication originale soit adéquatement citée, que l’utilisation se fasse à des fins non commerciales (c.-à-d., recherche ou éducation) et qu’aucune modification ni adaptation n’y soit apportée. Voir : https://creativecommons.org/licenses/by-nc-nd/4.0/