La thrombocytopénie thrombotique immunitaire induite par le vaccin (TTIV) doit être prise en considération chez tous les patients présentant des symptômes de thrombose et de thrombocytopénie après avoir récemment obtenu un vaccin contre le SRAS-CoV-2 qui fait appel à un vecteur adénovirus (ChAdOx1 nCoV-19 Oxford–AstraZeneca ou Ad26.COV2.S Johnson & Johnson–Janssen).
Le tableau clinique et la pathobiologie de la TTIV sont comparables à ceux de la thrombocytopénie induite par l’héparine (TIH), mais dans le cas de la TTIV, un anticorps de l’immunoglobuline G (IgG) dirigé contre le facteur plaquettaire 4 provoque l’activation plaquettaire, une thrombose et une thrombocytopénie.
Les tests de dépistage rapides de la TIH couramment utilisés, comme l’immunodosage d’agglutination au latex, peuvent donner un résultat faussement négatif chez les patients atteints d’une TTIV; cependant, les méthodes immunoenzymatiques à double détermination d’anticorps appliquées à la TIH et les dosages de libération de la sérotonine peuvent être employés pour détecter et confirmer la présence de TTIV, respectivement.
Si une TTIV est soupçonnée, l’administration d’héparine devrait être interrompue et remplacée par une anticoagulothérapie de remplacement; la transfusion de plaquettes devrait être évitée et l’administration d’immunoglobuline intraveineuse devrait être prise en considération pour les patients qui présentent des caractéristiques cliniques préoccupantes.
Un homme de 63 ans s’est présenté au service des urgences avec une jambe froide et douloureuse perdurant depuis 5 jours, une nouvelle manifestation de paresthésie de la jambe et du pied gauches et un grave essoufflement. Le patient n’avait pas d’antécédents personnels ou familiaux d’événements thrombotiques et aucun antécédent personnel ni symptôme d’arythmie. Il ne fumait pas et ne présentait pas de symptômes; il n’y avait pas de notes antérieures au dossier concernant des maladies vasculaires périphérique, coronarienne ou cérébrovasculaire. Il présentait des antécédents d’obésité et d’hypertension contrôlée par une monothérapie. Deux tests de dépistage cliniques rapides ont fourni un résultat négatif à la présence du SRAS-CoV-2 plus tôt le jour de la consultation (test de dépistage d’acides nucléiques isothermaux ID NOW d’Abbott). Le patient avait reçu une première dose du vaccin ChAdOx1 nCoV-19, 20 jours avant l’apparition des symptômes.
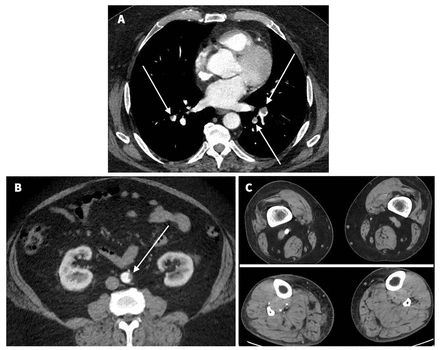
Lors de la consultation, nous avons observé que le patient était obèse (indice de masse corporel de 41,8) et en hypoxie (saturation en oxygène de 85 % à l’air ambiant, normale > 90 %). Son pied gauche était froid, pâle et insensible, présentant une fonction motrice diminuée et l’absence de signaux Doppler artériels (ischémie aiguë d’un membre de grade IIB de Rutherford)1. Les analyses de laboratoires ont révélé une thrombocytopénie (numération plaquettaire de 36 [normale 150–400] × 109/L), D-dimères > 10 000 (normale ≤ 50) ng/mL unités équivalentes fibrinogènes, fibrinogènes de 1,4 (normale 1,6–4,1) g/L et un rapport international normalisé de 1,3 (normale 0,9–1,1). Une angiographie par tomodensitométrie a décelé une occlusion de l’artère poplitée gauche sans vaisseaux tibiaux visibles, même en phase retardée. Elle a aussi montré des thrombus de l’artère pulmonaire segmentaire bilatérale et un thrombus adhérant à la paroi de l’aorte infrarénale (figure 1).
Angiographies par tomodensitométrie d’un homme de 63 ans présentant une thrombocytopénie thrombotique immunitaire induite par le vaccin, montrant (A) un thrombus de l’artère pulmonaire bilatérale, (B) un thrombus de l’aorte infrarénale et (C) un rehaussement de contraste normal des artères poplitée (coin supérieur droit) et tibiale (coin inférieur droit) de la jambe non ischémique droite; sans rehaussement des artères poplitée (coin supérieur gauche) et tibiale (coin inférieur gauche) de la jambe ischémique gauche.
Nous avons entrepris une anticoagulothérapie accompagnée d’héparine non fractionnée intraveineuse. Une thrombectomie chirurgicale d’urgence de l’artère poplitée et de l’ensemble des artères tibiales a produit une grande quantité de thrombus. Nous avons infusé un activateur tissulaire du plasminogène dans les artères tibiales pendant l’intervention chirurgicale. Nous avons obtenu un bon flux antérograde et rétrograde, avec une hyperémie du pied et des signaux Doppler artériels triphasiques normaux après reperfusion. Au cours de l’intervention chirurgicale, le patient souffrait d’hypoxie par intermittence, un état compatible avec l’important thrombus présent dans son artère pulmonaire.
L’évolution postopératoire de notre patient était compliquée par une hypoxie grave, une thrombocytopénie et un saignement important au site opératoire, pour lequel ont lui a administré de nombreuses transfusions sanguines et de plaquettes. Après 24 heures, l’hyperémie de l’avant-pied a évolué en cyanose, avec l’infarcissement subséquent des orteils, malgré l’administration d’héparine intraveineuse thérapeutique (temps de thromboplastine partielle 60–90 [normale ≤ 39] s). Nous n’avons pas observé de symptômes cliniques du syndrome des loges. Nous avons réalisé un dosage rapide de thrombocytopénie induite par l’héparine (TIH) à 3 reprises et tous les résultats étaient négatifs (immunodosage d’agglutination au latex HemosIL HIT-Ab(PF4-H)). Le patient n’avait pas d’antécédent d’exposition à l’héparine. Un dépistage d’anticorps antiphospholipides pour l’anticardiolipine, la glycoprotéine anti-β2 et l’anticoagulant lupique ainsi que des dosages d’un antigène nucléaire extractible, d’un anticorps antinucléaire, d’un facteur de rejet et de la mutation JAK2 V617F étaient négatifs. Un échocardiogramme postopératoire n’a pas démontré de persistance du foramen ovale cliniquement significative, ce qui selon nous a écarté la possibilité d’une embolie paradoxale.
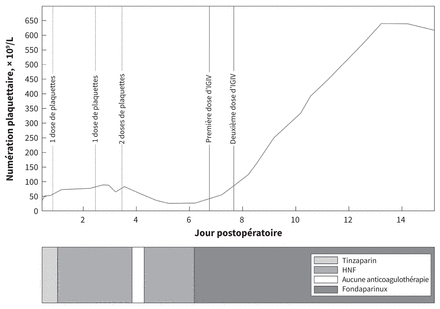
Nous avons soupçonné une thrombocytopénie thrombotique immunitaire induite par le vaccin (TTIV) sur la base d’un saignement postopératoire persistant, de nouvelles thromboses digitales et d’une thrombocytopénie qui ne répondait pas à la transfusion de plaquettes. Nous avons remplacé l’héparine non fractionnée par du fondaparinux (10 mg/j par voie sous-cutanée, la dose recommandée pour un poids corporel > 100 kg) et administré de l’immunoglobuline intraveineuse (1 g/kg/j) pendant 2 jours consécutifs (Gammunex). Par la suite, la thrombocytopénie du patient s’est rapidement améliorée (figure 2) et le saignement présent au site opératoire s’est résorbé.
Numération plaquettaire et anticoagulothérapie au cours de l’évolution clinique de la thrombocytopénie thrombotique immunitaire induite par le vaccin du patient. La numération plaquettaire ne réagissait pas à la transfusion plaquettaire. Un rétablissement important de la numération plaquettaire est survenu après l’administration d’immunoglobuline intraveineuse (IGIV). Remarque : HNF = héparine non fractionnée.
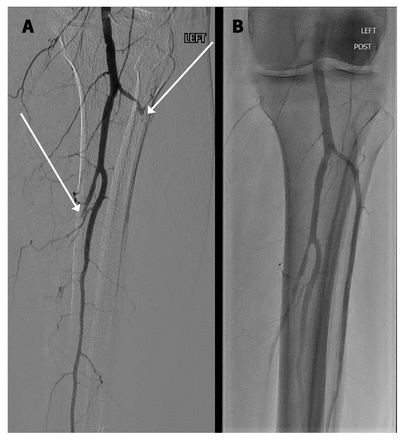
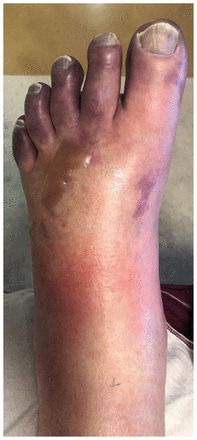
Nous avons confirmé une TTIV au jour 11 suivant l’intervention chirurgicale par une méthode immunoenzymatique à double détermination d’anticorps (ELISA) qui a permis de détecter la présence du facteur plaquettaire 4 du complexe de l’immunoglobuline dans le sérum du patient, et par un dosage de libération de la sérotonine qui a démontré une activation plaquettaire lorsque le facteur plaquettaire 4 était ajouté au sérum du patient, sans héparine (Laboratoire d’immunologie plaquettaire, Université McMaster, Hamilton, Ont.). Au jour postopératoire 15, des angiographies ont confirmé une remanifestation partielle de thromboses dans la circulation tibiale. Une thrombectomie par aspiration a contribué à retirer les nouvelles thromboses (figure 3), entraînant une reperfusion substantielle de l’avant-pied. Nous avons planifié une amputation transmétatarsienne une fois que l’avant-pied sera totalement délimité (figure 4).
Angiographie poplitée et tibiale de la jambe gauche du patient montrant (A) une remanifestation de thromboses postopératoires des artères tibiales antérieure et postérieure (flèches), puis (B) la recanalisation après une thrombectomie par aspiration.
Photographie de l’avant-pied gauche du patient montrant une ischémie au jour 14 suivant l’intervention.
Discussion
La TTIV est un syndrome qui a été signalé pour la première fois en avril 2021 chez des patients qui avaient récemment obtenu le vaccin ChAdOx1 nCoV-192–7. Elle ressemble fortement à la TIH, chez laquelle des anticorps, typiquement l’immunoglobuline G (IgG), sont produits contre les complexes formés du facteur plaquettaire 4 circulants et de l’héparine endogène8–10. Les plaquettes neutralisent l’héparine endogène et régulent l’hémostase en libérant le facteur plaquettaire 4, une protéine à 70 acides aminés qui se lie à l’héparine. Dans le cas de la TIH, l’anticorps IgG qui est lié au complexe héparine–facteur plaquettaire 4 se lie aussi aux récepteurs des plaquettes Fcγ, déclenchant une activation plaquettaire et favorisant la production de thomboses10. Quant à la TTIV, on croit que le vaccin mène à l’élaboration d’une IgG qui cible le facteur plaquettaire 4 (contrairement au complexe héparine–facteur plaquettaire 4), qui se lie aussi aux récepteurs Fcγ et active les plaquettes7. Bien que l’IgG n’ait pas besoin d’héparine pour activer les plaquettes dans le cas de la TTIV, la présence d’héparine pourrait l’aggraver, car les complexes héparine–facteur plaquettaire 4 peuvent aussi se lier à l’IgG issu de la TTIV comme à celle de la TIH.
Il est important de noter que les immunodosages d’agglutination au latex rapides contre la TIH utilisés dans notre laboratoire ne détectent pas la présence l’IgG impliquée dans la TTIV. Cependant, les dosages ELISA de la TIH détectent généralement l’IgG associée à la TTIV et devraient être exigés lorsqu’un cas de TTIV est soupçonné. Dans le cas de notre patient, nous avons finalement confirmé une TTIV par 2 dosages qui sont actuellement disponibles pour la TIH : un dosage ELISA pour le facteur plaquettaire 4 qui dépiste la présence de l’IgG de la TTIV et le dosage de libération de la sérotonine pour les plaquettes qui confirme la TTIV. En ce qui a trait à la TIH, les 2 dosages détectent les complexes héparine–facteur plaquettaire 4–IgG–polyanion. Le dosage de libération de la sérotonine induit l’activation plaquettaire en mesurant la libération de sérotonine lorsque le sérum du patient qui contient de l’IgG est incubé avec de l’héparine9. Dans le cas de la TTIV, le dosage de libération de la sérotonine détecte l’IgG antifacteur plaquettaire 4 sans ajout d’héparine11.
L’immunoglobuline intraveineuse est l’une des thérapies suggérées pour les patients atteints de la TTIV qui ont un tableau clinique préoccupant comme des saignements et la formation continue de thromboses, comme dans le cas de la TIH. Nous sommes d’avis que cette thérapie a finalement contribué à l’amélioration de l’état de santé de notre patient. Notre décision d’employer de l’immunoglobuline intraveineuse n’était pas fondée sur sa numération plaquettaire, mais sur le tableau clinique présenté par le saignement continu et la thrombose qui se poursuivaient malgré le retrait de l’héparine. À la fois dans le cas de la TIH et la TTIV, on croit que le mécanisme d’action de l’immunoglobuline intraveineuse entre en compétition pour se lier au récepteur Fcγ avec l’IgG dérivée de l’immunoglobuline intraveineuse qui n’active pas les plaquettes12,13.
C’est sans surprise que nous avons observé que le retrait de l’héparine non fractionnée et sa substitution pour le fondaparinux, 6 jours après le début de l’hospitalisation (figure 2), n’a pas immédiatement freiné la thrombocytopénie et le saignement de notre patient. La capacité de l’IgG associée à l’TTIV de le lier au facteur plaquettaire 4 sans avoir recours au complexe héparine–facteur plaquettaire 4 en est probablement la cause7. Cependant, les cliniciens devraient interrompre l’héparine (ou ne pas l’utiliser du tout) chez les patients atteints de TTIV, puisqu’une diminution des taux de complexes héparine–facteur plaquettaire 4 peut mener à une quantité moindre d’antigènes du facteur plaquettaire 4 circulants.
Dans notre cas, nous avons procédé à une thrombectomie chirurgicale d’urgence en raison de la gravité de l’ischémie du membre. Bien que nous ayons observé une excellente reperfusion précoce de l’extrémité ischémique, le fait de ne pas avoir reconnu la TTIV du patient a probablement mené à des thromboses et à l’infarcissement des orteils, malgré une dose de fondaparinux ajustée selon le poids. Les transfusions de plaquettes administrées pour traiter le saignement peuvent avoir aggravé les thromboses en fournissant davantage de réactifs aux anticorps associés à la TTIV pour le déclenchement de la formation de caillots. Une reconnaissance et un traitement précoces de la TTIV à l’aide d’immunoglobuline intraveineuse auraient pu diminuer les thromboses après ce qui apparaît être une thrombectomie chirurgicale réussie. Enfin, l’incapacité de notre immunodosage d’agglutination au latex de la TIH à détecter les anticorps de la TTIV contre le facteur plaquettaire 4 a contribué à ce diagnostic tardif.
Les premiers cas publiés de TTIV décrivent surtout des thromboses veineuses atypiques telles que des thromboses veineuses cérébrales et des thromboses des veines splanchniques chez des jeunes femmes en bonne santé, 5–16 jours après la première dose du vaccin ChAdOx1 nCoV-192,3. Dans le cadre d’une étude, tous les patients atteints de TTIV étaient des travailleurs de la santé d’origine norvégienne de moins de 65 ans, dont 80 % étaient des femmes; au moment de l’étude, cette population était vaccinée de préférence avec ce vaccin en Norvège3. Ces premiers rapports ne constituent peut-être pas un portrait exact de la véritable distribution démographique et du comportement clinique de la TTIV. Un article récent publié au Royaume-Unis est plus représentatif de la population générale qui a obtenu le vaccin ChAdOx1 nCoV-19. Il cible la TTIV chez un groupe beaucoup plus élargi de personnes de 21–77 ans, dont 60 % étaient des femmes7. Notre patient était un homme d’âge moyen dont les symptômes se sont manifestés 20 jours après l’administration de la première dose du vaccin et il s’est présenté avec des thromboses dans de multiples lits vasculaires. Des articles récents publiés par Thrombose Canada et la Société internationale de thrombose et d’hémostase fournissent les critères diagnostics et des renseignements sur le traitement de la TTIV14,15. Ils montrent que les patients qui en sont atteints peuvent présenter une large gamme d’événements thrombotiques et ils ne ciblent aucun critère diagnostique fondé sur l’âge ou le sexe. Deux récents rapports ont aussi décrit la TTIV chez des patients qui ont reçu le vaccin Ad26.COV2.S (Johnson & Johnson–Janssen)6,16; la Société internationale de thrombose et d’hémostase cible ces 2 vaccins qui font appel à des vecteurs adénovirus (ChAdOx1 nCoV-19 et Ad26.COV2.S) comme des déclencheurs potentiels de la TTIV15.
Conclusion
Tous les médecins devraient connaître l’existence de la TTIV, compte tenu de l’utilisation actuelle des vaccins ChAdOx1 nCoV-19 et Ad26.COV2.S contre le SRAS-CoV-2. Cette pathologie doit être prise en considération chez tous les patients présentant des symptômes de thrombose et de thrombocytopénie après avoir récemment obtenu un vaccin contre le SRAS-CoV-2 qui fait appel à un vecteur adénovirus. Plusieurs observations cliniques de la TTIV sont comparables à la TIH, mais des immunodosages rapides pour la TIH, comme l’immunodosage d’agglutination au latex, donnent souvent des résultats faussement négatifs chez les patients atteints de TTIV. Par ailleurs, les dosages ELISA utilisés pour la TIH peuvent détecter l’immunoglobuline G (IgG) associée à la TTIV et le dosage de libération de la sérotonine confirme la TTIV si le sérum du patient déclenche l’activation plaquettaire lorsqu’il est incubé sans héparine. Finalement, si on soupçonne une TTIV, l’héparine ne devrait pas être utilisée et une anticoagulothérapie sans héparine, comme le fondaparinux, l’argatroban ou un anticoagulant oral direct, devrait plutôt être administrée. Pour les patients présentant des saignements rebelles, des thromboses qui se poursuivent ou d’autres caractéristiques inquiétantes, l’administration d’immunoglobuline par voie intraveineuse peut être utile.
La section Études de cas présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs : www.cmaj.ca.
Remerciements
Les auteurs remercient les Dres Tania Pannu et Elizabeth Mackay et le Dr Jeffrey Shrum pour leur expertise et leur soutien dans les soins prodigués à ce patient. Ils remercient aussi le personnel du Laboratoire d’immunologie plaquettaire de l’Université McMaster (Hamilton, Ont.) pour le test de dépistage et l’interprétation de ses résultats qui ont confirmé le diagnostic de thrombocytopénie thrombotique immunitaire induite par le vaccin.
Footnotes
Voir la version anglaise de l’article ici : www.cmaj.ca/lookup/doi/10.1503/cmaj.210795; voir le commentaire connexe en français au www.cmaj.ca/lookup/doi/10.1503/cmaj.210882-f, et en anglais au www.cmaj.ca/lookup/doi/10.1503/cmaj.210882
Intérêts concurrents: Aucun déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement du patient.
Collaborateurs: Tous les auteurs ont contribué à l’élaboration et à la conception du travail ainsi qu’à la collecte des données. Melissa Jones, Annie Boisvert et Paul Petrasek ont analysé les données et contribué à l’ébauche du manuscrit. Tous les auteurs ont révisé de façon critique son contenu intellectuel important, ont donné leur approbation finale pour la version destinée à être publiée et endossent l’entière responsabilité de tous les aspects du travail.
Il s’agit d’un article en libre accès distribué conformément aux modalités de la licence Creative Commons Attributions (CC BY-NC-ND 4.0), qui permet l’utilisation, la diffusion et la reproduction dans tout médium à la condition que la publication originale soit adéquatement citée, que l’utilisation se fasse à des fins non commerciales (c.-à-d. recherche ou éducation) et qu’aucune modification ni adaptation n’y soit apportée. Voir : https://creativecommons.org/licenses/by-nc-nd/4.0/deed.fr