La blessure à l’épaule liée à l’administration d’un vaccin (ou SIRVA, pour shoulder injury related to vaccine administration) est un événement rare qui peut être lié à la vaccination anti-SRAS-CoV-2.
Chez les patients qui consultent pour une douleur persistante à l’épaule et une réduction de leur amplitude de mouvement peu après avoir reçu un vaccin anti-SRAS CoV 2, les médecins devraient inclure la SIRVA dans leurs diagnostics différentiels, avec l’arthrite septique.
Les patients atteints d’une SIRVA présentent habituellement une bursite sous-acromiale que l’on détecte à l’échographie; si on y a accès, l’imagerie par résonance magnétique se révèle plus sensible.
On peut réduire le risque de SIRVA en injectant le vaccin selon la technique appropriée, ce qui inclut choisir une aiguille de la bonne longueur pour le patient, bien la positionner et éviter une pénétration excessive au tiers supérieur du muscle deltoïde.
Cas 1
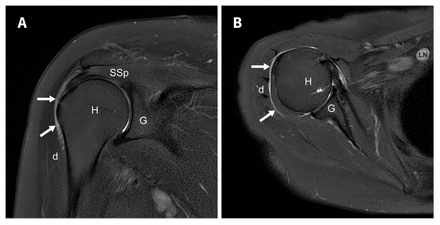
Une femme de 62 ans ayant des antécédents d’hypertension, de dyslipidémie et de douleur cervicale, mais n’ayant aucun antécédent de douleur à l’épaule a reçu sa première dose de vaccin ChAdOx1 nCoV-19. Elle a déclaré avoir senti que l’aiguille avait été insérée plus haut dans son bras comparativement à de précédents vaccins, et ressenti une douleur durant l’injection. Immédiatement après l’injection, elle a présenté une diminution de son amplitude de mouvement (ADM) à l’épaule droite et l’élévation et l’abduction actives de son bras droit étaient limitées à 45°, ce qui rendait difficile l’exécution de ses tâches quotidiennes. Deux semaines après l’administration du vaccin, son médecin de famille a demandé une échographie de l’épaule qui a montré une légère distension de la bourse sous-acromiale et une trace de liquide avasculaire dans la bourse sous-deltoïdienne antérieure, sans accumulation de liquide au niveau du muscle deltoïde ni anomalie des tendons ou de l’articulation. Comme son état clinique ne s’était toujours pas amélioré 1 mois après la vaccination, la patiente a subi une épreuve d’imagerie par résonance magnétique (IRM) de son épaule droite au privé, qui a montré une distension et une inflammation focales des aspects inférieur et latéral de la bourse sousdeltoïdienne évoquant une bursite au point d’injection de son vaccin (figure 1). On n’a identifié aucune autre cause de sa douleur aiguë. L’imagerie a montré une arthrose de l’articulation acromioclaviculaire et une légère tendinose de la coiffe des rotateurs, phénomène prévisible vu son âge.
Clichés d’imagerie par résonance magnétique avec suppression du signal des tissus adipeux chez une femme de 62 ans présentant une blessure à l’épaule liée à l’administration d’un vaccin (SIRVA, pour shoulder injury related to vaccine administration), où on observe une bursite sous-deltoïdienne. (A) Clichés coronal et (B) axial qui montrent une distension et une inflammation focales des aspects inférieur et latéral de la bourse sous-deltoïdienne (flèches). Le cliché axial montre aussi une lymphadénopathie axillaire, probablement réactive. D = deltoïdien, G = glénoïdal, H = humérus, LN = ganglion lymphatique, SSp = supraspinatus.
Le médecin de famille de la patiente a géré ses symptômes de manière conservatrice, sans physiothérapie formelle ni injections de corticostéroïdes. Sa douleur a fini par rentrer dans l’ordre. Huit semaines après l’administration du vaccin, l’ADM de son épaule s’était améliorée et la patiente arrivait à effectuer la majeure partie de ses tâches quotidiennes. Une douleur sourde a persisté au point d’injection, sans nécessiter d’analgésiques. À la semaine 12, ses symptômes avaient disparu et elle a reçu sa deuxième dose de vaccin ChAdOx1 nCoV-19 sans difficulté.
Cas 2
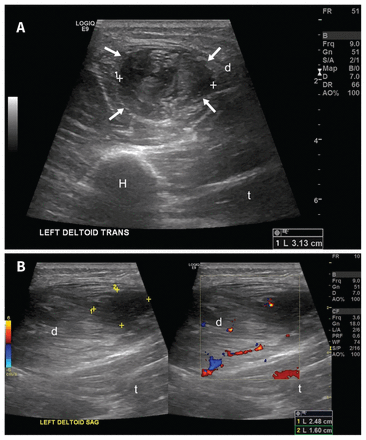
Un homme de 63 ans ayant des antécédents d’arthrose aux membres inférieurs et de fibrillation auriculaire paroxystique (ne nécessitant pas de traitement) a reçu sa première dose de vaccin ChAdOx1 nCoV-19 sans complications immédiates. Quatre semaines plus tard, il a reçu sa seconde dose du même vaccin sans problème. Deux semaines après la deuxième dose, il a toutefois présenté une douleur et une enflure progressives à la partie supérieure du bras gauche près du point d’injection, entraînant une légère restriction de l’ADM de l’épaule. Il pouvait encore s’adonner à ses activités quotidiennes régulières. Il a déclaré que le point d’injection du vaccin était similaire à ceux de vaccins précédents. Les échographies de son épaule gauche effectuées après qu’il ait consulté aux urgences ont montré une zone kystique complexe à l’intérieur du muscle deltoïde gauche mesurant 31 × 25 × 16 mm (figure 2). On n’a noté aucune extension vers la portion profonde du muscle ou des tissus sous-cutanés, aucune hyperémie associée n’a suggéré un processus infectieux et on n’a noté aucune distension de la bourse sous-deltoïdienne. Le rapport de radiologie a fait état d’une quantité trace de liquide simple à la surface du muscle deltoïdien. Ces observations concordent avec un hématome intramusculaire subaigu, secondaire à la récente administration du vaccin. Le médecin de famille du patient a géré ses symptômes de manière conservatrice avec acétaminophène, anti-inflammatoires non stéroïdiens, glace et massothérapie. La douleur est graduellement rentrée dans l’ordre au cours des 4 semaines suivantes. À la septième semaine de suivi, le patient continuait de sentir une masse palpable, quoique de moindre envergure, au haut du bras gauche. Toutefois, la douleur était complètement rentrée dans l’ordre sans restrictions aux plans de l’ADM ou des activités quotidiennes.
Échographies chez un homme de 63 ans présentant une SIRVA. Clichés (A) transverse et (B) sagittal qui montrent une zone kystique complexe au muscle deltoïdien gauche (flèches) mesurant 31 × 25 × 16 mm. D = deltoïdien, H = humérus, T = triceps.
Discussion
Le National Vaccine Injury Compensation Program des États-Unis définit la blessure à l’épaule liée à l’administration d’un vaccin (ou SIRVA, pour shoulder injury related to vaccine administration) comme un « événement indésirable consécutif à la vaccination qui serait liée à la technique d’injection intramusculaire percutanée dans le bras entraînant un traumatisme causé par l’aiguille et/ou l’injection involontaire du vaccin dans les tissus et les structures sousdeltoïdiennes de l’épaule »1. Nous présentons ici 2 cas de SIRVA consécutifs à l’administration d’un vaccin contre le SRAS-CoV 2: 1 cas de bursite sous-deltoïdienne et 1 cas d’hématome intramusculaire. Même si l’hématome intramusculaire est une manifestation moins fréquente de la SIRVA, comparativement à la bursite, il pourrait être dû à une lésion des vaisseaux intramusculaires causée par l’insertion de l’aiguille lors de la vaccination.
Causes et facteurs de risque
La SIRVA est une complication iatrogène rare et souvent évitable. On dispose de peu de données épidémiologiques sur le sujet et les cas sont peut-être sous-déclarés. Nous avons recensé 61 cas de SIRVA lors d’une revue de la littérature semi-structurée et nous avons résumé les symptômes, les vaccins administrés et l’évolution clinique (annexe 1, accessible en anglais au www.cmaj.ca/lookup/doi/10.1503/cmaj.211162/tab-related-content) pour chacun. À l’heure actuelle, 6 cas de SIRVA liés à des vaccins anti-SRAS-CoV-2 ont été publiés en plus des 2 nôtres, dont 1 au Brésil et 1 en Thaïlande liés au vaccin ChAdOx1 nCoV-19, 1 second cas en Thaïlande lié au vaccin Sinovac–CoronaVac et 3 cas aux États-Unis liés aux vaccins à ARN messager (mRNA 1273 et BNT162b2) (annexe 1). Les données disponibles ne permettent pas d’associer la SIRVA à des vaccins en particulier et le risque de SIRVA est probablement équivalent, peu importe le vaccin.
On ignore la cause exacte de la SIRVA, mais il pourrait s’agir d’une réaction immunitaire aux antigènes viraux et aux adjuvants des vaccins2. La réponse inflammatoire n’est pas spécifique aux vaccins, mais selon une théorie, elle serait causée par l’exposition d’un patient déjà sensibilisé à l’antigène viral, soit par transmission naturelle, soit lors de vaccinations précédentes. Comme le récent cas du Brésil, la première patiente que nous présentons dans ce rapport a manifesté une SIRVA après sa première dose vaccin ChAdOx1 nCoV-19. Selon notre hypothèse, la patiente avait été exposée au SRAS-CoV-2 ou à un adénovirus contenu dans le vaccin ChAdOx1 nCoV-19 (annexe 1).
Une autre source potentielle de douleur à l’épaule liée à la SIRVA est la présence d’une pathologie préexistante mais asymptomatique à l’épaule qui se trouve activée par le traumatisme ou la blessure causés par l’injection du vaccin2. Selon notre expérience, la distension et l’inflammation de la bourse sous-deltoïdienne inférolatérale sont dues à l’administration involontaire du vaccin à cet endroit; et les épreuves d’imagerie donnent des résultats différents de ce que l’on observe typiquement avec le syndrome d’accrochage sous-acromial. Cela évoque un élément d’irritation locale dû à la technique d’injection du vaccin ou à son injection involontaire dans la bourse plutôt que dans le muscle.
La plupart des cas de SIRVA signalés dans la littérature affectent des femmes (annexe 1). Cela serait lié à leur morphologie, car la masse musculaire du deltoïde est plus faible chez la femme que chez l’homme, ce qui l’expose à des blessures causées par des aiguilles plus longues ou par une piètre technique. La majorité des patients présentant une SIRVA confirmée ont déclaré avoir ressenti une douleur à l’épaule au point d’injection et avoir senti que l’injection avait été effectuée plus haut sur le muscle deltoïde. Le tableau clinique de la première patiente ressemble à celui d’autres cas de SIRVA liés à une bursite signalés dans la littérature. Toutefois, nous n’avions encore jamais entendu parler d’un hématome intramusculaire lié à la SIRVA, comme chez notre deuxième patient.
Tableau clinique et diagnostic
La SIRVA peut avoir un impact négatif sur la qualité de vie des patients. La plupart des patients font état d’une douleur intense au cours des 48 premières heures et chez certains, les symptômes ont pris jusqu’à 2 mois avant de se manifester3. La diminution de l’ADM de l’épaule est fréquente; la faiblesse, une altération de la sensibilité et la fièvre le sont moins2. Les diagnostics différentiels de la SIRVA incluent arthrite septique, inflammation locale (p. ex., bursite, capsulite adhésive, tendinite), atteinte nerveuse (p. ex., atteinte du nerf axillaire), syndrome d’accrochage sous-acromial et traumatisme (c. à d., déchirure de 1 ou plusieurs tendons de la coiffe des rotateurs). Dans de rares cas, une érosion osseuse, l’ostéonécrose de la tête humérale, l’arthrose septique et la chondrolyse progressive ont été rapportées4–7.
Les médecins devraient rechercher les signes d’une infection systémique, par exemple, fièvre, douleurs articulaires, oedème et érythème. Les analyses de laboratoire qui montrent une hausse de la numération leucocytaire et des marqueurs de l’inflammation (tels que protéine C réactive, vitesse de sédimentation des érythrocytes ou viscosité plasmatique) pourraient suggérer une pathologie infectieuse plutôt qu’un processus inflammatoire. Si les symptômes de douleur à l’épaule et de restriction de l’ADM ne sont pas rentrés dans l’ordre 1 semaine après l’administration du vaccin, nous recommandons des radiographies de l’épaule pour écarter d’autres causes de douleur, et des épreuves d’imagerie (échographie ou IRM) des tissus mous pour dépister une bursite. Lorsqu’on détecte une bursite sous-acromiale, l’échographie a une sensibilité de 0,79 à 0,81 et une spécificité de 0,94 à 0,988. Toutefois, l’échographie dépend de l’opérateur et pourrait sous-estimer les signes en raison d’une pression directe exercée durant l’examen; l’IRM offre une sensibilité plus grande pour la détection des pathologies de l’épaule9.
Chez la première patiente, l’épaississement de la bourse n’a pas été détecté à l’échographie, mais bien à l’IRM. La localisation sousdeltoïdienne de l’épaississement de la bourse est atypique pour une bursite sous-acromiale courante et peut être subtile, ce qui rend sa détection à l’échographie plus difficile. On peut donc envisager une IRM si elle est indiquée au plan clinique et si les résultats de l’échographie ne concordent pas avec le tableau clinique.
Traitement et prévention
Chez les patients qui présentent une bursite confirmée à l’imagerie, le traitement reposera sur des modifications à l’hygiène de vie et aux conditions de travail, sur la physiothérapie et les anti-inflammatoires non stéroïdiens. Des injections de corticostéroïdes peuvent être envisagées si les symptômes sont graves et ne répondent pas aux mesures conservatrices2. Les patients qui ont une bursite sous-deltoïdienne, une bursite sous-acromiale ou un hématome intramusculaire liés à la SIRVA peuvent être rassurés car leurs symptômes à l’épaule rentreront fort probablement dans l’ordre et leur état s’améliorera progressivement en 4–6 semaines10. Aucune chirurgie n’est habituellement requise.
Pour prévenir la SIRVA, les injections intramusculaires à la partie supérieure du bras devraient généralement éviter une pénétration excessive au tiers supérieur du muscle deltoïde, étant donné que les bourses sous-acromiales peuvent avoir une profondeur de 0,8–1,6 cm sous la surface de la peau et s’étendre jusqu’à 3–6 cm sous la limite latérale de l’acromion10. Les injections administrées trop superficiellement peuvent nuire à l’efficacité du vaccin et accroître l’inconfort du patient11. Une pénétration excessive causée par une aiguille trop longue pour la morphologie du patient ou une piètre technique d’administration peuvent endommager les vaisseaux et les nerfs avoisinants (p. ex., branche antérieure du nerf axillaire et des vaisseaux circonflexes huméraux postérieurs), des bourses (p. ex., bourses sous-acromiale et sous-deltoïdienne) et des tendons (p. ex., coiffe des rotateurs), ou peuvent entraîner un processus infectieux nécessitant une irrigation et un débridement chirurgicaux (annexe 1).
Conformément aux recommandations actuelles des fabricants en ce qui concerne la pratique et la vaccination, nous suggérons d’asseoir le patient à la même hauteur que la personne qui lui administre le vaccin et de rendre bien visible le muscle deltoïde, avec le bras au repos sur le côté2,12. La personne qui administre le vaccin devrait choisir une longueur d’aiguille adaptée à l’âge, au sexe, à l’indice de masse corporelle du patient, ainsi qu’à l’épaisseur des tissus sous-cutanés3. L’aiguille doit être perpendiculaire à la peau et entrer à 2 ou 3 doigts de distance du processus acromial, évitant de ce fait le tiers supérieur du muscle deltoïde12. Une autre méthode qui a déjà été suggérée pour éviter de blesser la bourse sous-acromiale ou sous-deltoïdienne lors de l’administration d’un vaccin consiste à placer la main du patient sur sa hanche ipsilatérale (ce qui provoque une légère abduction de l’épaule) et à adopter un point à mi-chemin entre l’acromion latéral et la tubérosité deltoïdienne 13.
La section Études de cas présente de brefs rapports de cas à partir desquels des leçons claires et pratiques peuvent être tirées. Les rapports portant sur des cas typiques de problèmes importants, mais rares ou sur des cas atypiques importants de problèmes courants sont privilégiés. Chaque article commence par la présentation du cas (500 mots maximum), laquelle est suivie d’une discussion sur l’affection sous-jacente (1000 mots maximum). La soumission d’éléments visuels (p. ex., tableaux des diagnostics différentiels, des caractéristiques cliniques ou de la méthode diagnostique) est encouragée. Le consentement des patients doit impérativement être obtenu pour la publication de leur cas. Renseignements destinés aux auteurs: www.cmaj.ca.
Footnotes
Voir la version anglaise de l’article ici: www.cmaj.ca/lookup/doi/10.1503/cmaj.211162
Intérêts concurrents: Jacky Chow est coprésident du consortium étudiant de l’International Society of Photogrammetry and Remote Sensing. Aucun autre intérêt concurrent n’est déclaré.
Cet article a été révisé par des pairs.
Les auteurs ont obtenu le consentement des patients.
Collaborateurs: Tous les auteurs ont contribué à la conception du travail, ont rédigé le manuscrit et en ont révisé de façon critique le contenu intellectuel important; ils ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
Avis: Les 2 cas ont été signalés à Vigilance Canada.
Il s’agit d’un article en libre accès distribué conformément aux modalités de la licence Creative Commons Attribution (CC BY-NC-ND 4.0), qui permet l’utilisation, la diffusion et la reproduction dans tout médium à la condition que la publication originale soit adéquatement citée, que l’utilisation se fasse à des fins non commerciales (c.-à-d., recherche ou éducation) et qu’aucune modification ni adaptation n’y soit apportée. Voir: https://creativecommons.org/licenses/by-nc-nd/4.0/