Le syndrome de tachycardie orthostatique posturale (STOP) est un trouble multisystémique chronique dont le symptôme cardinal est une tachycardie orthostatique.
Les patients atteints de STOP ont des symptômes d’intolérance orthostatique qui s’améliorent en décubitus.
Les filles et les femmes sont plus sujettes au STOP, de la puberté jusqu’au début de l’âge adulte.
Le STOP peut nuire grandement aux capacités fonctionnelles et limite souvent la vie professionnelle ou la fréquentation scolaire.
Le traitement du STOP peut améliorer les symptômes et la capacité fonctionnelle et il peut être pris en charge en médecine de soins primaires.
La principale caractéristique du syndrome de tachycardie orthostatique posturale (STOP) est la tachycardie en position debout, sans chute de tension artérielle. Les patients parlent d’étourdissements et de palpitations lorsqu’ils sont en position redressée, particulièrement à la station debout, ce qui peut mener à la syncope. Les patients peuvent éprouver une baisse de leur qualité de vie et de leur capacité fonctionnelle qui peut avoir des conséquences économiques désastreuses1–3. Le syndrome est plus fréquent chez les filles et les jeunes femmes et il a été associé à d’autres maladies, comme la migraine et le syndrome d’Ehlers–Danlos4. Nous abordons le diagnostic du STOP, les maladies à inclure dans le diagnostic différentiel, les troubles associés et les traitements pharmacologiques et non pharmacologiques pour les patients atteints de STOP, sur la base de recherches originales, de revues narratives et d’énoncés consensuels (encadré 1).
Données utilisées pour la présente revue
Nous avons passé en revue les énoncés de position récents sur le diagnostic et le traitement du syndrome de tachycardie orthostatique posturale (STOP), notamment l’énoncé consensuel 2011 de l’American Autonomic Society, l’énoncé scientifique 2015 de la Heart Rhythm Society et l’énoncé de position 2020 de la Société canadienne de cardiologie. Pour les articles qui décrivent les mécanismes et les traitements spécifiques, nous avons interrogé le réseau MEDLINE jusqu’à juillet 2021, en utilisant les termes de langue anglaise suivants: « POTS », « postural tachycardia syndrome » et « postural orthostatic tachycardia syndrome ». Nous avons retenu principalement les articles originaux, mais également des articles de synthèse. Nous avons en outre exploré les listes bibliographiques des articles pertinents pour y trouver d’autres sources intéressantes.
Comment définit-on le STOP?
Plusieurs sociétés professionnelles en Amérique du Nord ont publié des critères établis par voie de consensus pour le diagnostic du STOP, notamment l’American Autonomic Society6, la Heart Rhythm Society7, la Société canadienne de cardiologie5 et, plus récemment, un groupe de travail sur le STOP des National Institutes of Health des États-Unis8. Les énoncés consensuels s’entendent sur le fait que la tachycardie orthostatique et l’intolérance orthostatique symptomatique doivent coexister et être chroniques. Les critères diagnostiques du STOP sont énumérés dans l’encadré 2. Les symptômes doivent se manifester à la station debout, après une accélération marquée de la fréquence cardiaque, mais sans chute substantielle de la tension artérielle. La présence d’autres problèmes de santé susceptibles d’expliquer la tachycardie orthostatique (tels qu’anémie, anxiété, fièvre, douleur, infection, déshydratation, hyperthyroïdie, phéochromocytome, alitement prolongé ou prise d’agents qui accélèrent la fréquence cardiaque, comme les stimulants, les diurétiques et les inhibiteurs de la recapture de la noradrénaline)9 permet d’écarter un diagnostic de STOP.
Critères diagnostiques du syndrome de tachycardie orthostatique posturale
Tous les critères suivants doivent être présents:
Accélération soutenue de la fréquence cardiaque de ≥ 30 battements/min (ou de ≥ 40 battements/min chez les patients de 12–19 ans) dès les 10 premières minutes en position debout
Absence d’hypotension posturale significative (ampleur de la baisse tensionnelle ≥ 20/10 mm Hg)
Aggravation des symptômes très fréquents d’intolérance orthostatique en position debout, avec amélioration rapide dès le retour au décubitus. Les symptômes varient d’un individu à l’autre, mais incluent souvent étourdissements, palpitations, tremblements, faiblesse généralisée, vision trouble et fatigue.
Durée des symptômes ≥ 3 mois
Absence d’autres problèmes de santé pouvant expliquer la tachycardie sinusale (encadré 3)
La tachycardie orthostatique doit survenir en l’absence d’hypotension posturale classique, mais une hypotension posturale initiale transitoire10 n’exclut pas un diagnostic de STOP5. La fréquence cardiaque du patient devrait s’accélérer d’au moins 30 battements/min (ou de ≥ 40 battements/min si le patient est âgé de 12–19 ans) lors d’au moins 2 mesures consécutives, à au moins 1 minute d’intervalle (encadré 2). L’énoncé de la Société canadienne de cardiologie5 établit la fréquence cardiaque minimale en position couchée à 60 battements/min pour exclure le diagnostic de STOP chez un patient dont la fréquence cardiaque est lente au repos et devient normale à la station debout.
Il est physiologiquement normal que la tachycardie orthostatique fluctue légèrement d’un jour à l’autre et qu’il y ait une variabilité diurne caractérisée par une tachycardie orthostatique plus marquée le matin comparativement au reste de la journée11. Si un médecin soupçonne fortement un STOP, mais que le patient ne répond pas aux critères de tachycardie orthostatique lors d’un examen initial, il est prudent de procéder à un examen de contrôle ultérieur, préférablement le matin.
Épidémiologie et histoire naturelle du STOP
Le syndrome de tachycardie orthostatique posturale est l’un des plus fréquents troubles du système nerveux autonome; on estime sa prévalence à 0,1 %–1 %1,12,13. Il affecte généralement les adolescentes et les jeunes femmes4, de sorte que la prévalence est plus élevée chez cette population et plus faible chez les hommes et les personnes âgées. Le syndrome de tachycardie orthostatique posturale est un syndrome hétérogène et plusieurs étiologies peuvent entraîner un phénotype clinique similaire. Même si les symptômes orthostatiques sont obligatoires pour le diagnostic, d’autres symptômes et caractéristiques cliniques diffèrent d’un patient à l’autre et les symptômes peuvent être communs à d’autres syndromes cliniquement définis8.
On dispose de peu de données probantes sur l’histoire naturelle à long terme du STOP. Chez les enfants, l’intolérance orthostatique semble s’améliorer avec le temps et le traitement, même si l’issue à long terme semble moins favorable quand les symptômes ont duré plus longtemps avant d’être pris en charge14. Il n’existe pas de données sur l’histoire naturelle chez les adultes; l’expérience clinique suggère que les symptômes et la capacité fonctionnelle peuvent s’améliorer avec le traitement, mais beaucoup n’obtiennent pas de rémission permanente3,15.
Quels autres problèmes de santé peuvent causer l’intolérance orthostatique?
Les médecins ou les patients peuvent confondre à tort le STOP avec d’autres problèmes de santé s’ils ne s’attardent qu’à l’intolérance orthostatique symptomatique ou à la tachycardie orthostatique excessive. Les patients sujets aux syncopes vasovagales peuvent présenter des épisodes répétés d’étourdissements en position debout en plus d’évanouissements occasionnels. Ces patients ont en général des signes vitaux orthostatiques normaux, mais certains ont aussi une tachycardie sinusale orthostatique16.
Les patients qui manifestent une baisse de tension posturale de 20 mm Hg ou plus peuvent présenter des symptômes d’intolérance orthostatique et parfois aussi une tachycardie orthostatique, mais l’hypotension posturale permet d’écarter le diagnostic de STOP6. L’hypotension posturale initiale s’observe plus souvent chez les adolescents et les jeunes adultes et peut provoquer des étourdissements dès l’adoption de la station debout, mais les symptômes rentrent dans l’ordre dans les 45 secondes qui suivent l’immobilisation en position debout.
Certains patients ont des symptômes d’intolérance orthostatique en l’absence de tachycardie et d’hypotension posturale et on en ignore la cause. Dans l’énoncé de la Société canadienne de cardiologie, ces patients sont jugés atteints de « symptômes posturaux sans tachycardie »5.
Les patients qui présentent une tachycardie orthostatique ne souffrent pas tous de STOP. La plupart des patients atteints de STOP ont une fréquence cardiaque au repos normale ou normale-elevee17. Si les patients ont une tachycardie constante, indépendamment de la position du corps, ils souffrent peut-être de tachycardie sinusale inappropriée. La tachycardie sinusale inappropriée doit obligatoirement être caractérisée par une fréquence cardiaque au repos qui demeure à au moins 100 battements/min ou une fréquence cardiaque moyenne des 24 heures supérieure à 90 battements/min. Les patients qui ont une tachycardie sinusale inappropriée ont des symptômes incommodants, sans cause sousjacente claire7. Si la tachycardie est due à un autre problème de santé causant une tachycardie sinusale (voir l’encadré 3), le diagnostic est une « tachycardie posturale d’étiologie autre »5.
Autres problèmes de santé pouvant expliquer la tachycardie sinusale en position debout5
Hypovolémie aiguë (par déshydratation ou perte sanguine)
Anémie
Hypotension posturale
Endocrinopathie
Insuffisance surrénalienne
Tumeur carcinoïde
Hyperthyroïdie
Phéochromocytome
Effets indésirables de médicaments
Crises de panique et anxiété grave
Repos ou alitement prolongé
Effets de drogues à usage récréatif
Enfin, les patients atteints de STOP ont une tachycardie sinusale et sans autres tachyarythmies supraventriculaires. Les médecins doivent envisager une tachycardie supraventriculaire paroxystique, surtout si elle n’est pas toujours positionnelle, si elle débute et cesse subitement (la fréquence cardiaque augmente habituellement plus graduellement avec un STOP), ou si la tachycardie répond à la manœuvre de Valsalva.
Quels autres problèmes de santé s’observent fréquemment chez les patients atteints de STOP?
Les patients atteints de STOP peuvent présenter d’autres symptômes et diagnostics concomitants; on ignore si ce sont des sous-ensembles physiopathologiques définitoires du STOP. La céphalée et les troubles du sommeil sont les plus fréquents. Les patients atteints de STOP ont souvent une intolérance à l’effort, plus de 90 % souffrent de fatigue chronique et au moins la moitié répondent aux critères d’encéphalomyélite myalgique/syndrome de fatigue chronique (EM/SFC)18. Un symptôme particulièrement invalidant est le « brouillard cérébral », une atteinte cognitive subjective19 qui s’aggrave souvent en position debout20. Nausées, ballonnements et troubles fonctionnels intestinaux sont fréquents. Un autre signe courant est l’acrocyanose périphérique des membres inférieurs en position debout. Les comorbidités souvent observées avec le STOP4,21 incluent le syndrome d’Ehlers–Danlos de type hypermobile, le syndrome d’activation mastocytaire22, la migraine et l’EM/SFC (tableau 1)18.
Comorbidités associées au syndrome de tachycardie orthostatique posturale*
La fréquence estimée de ces associations cliniques varie et la qualité des données les concernant est faible. Selon les données tirées d’autoquestionnaires4, environ 40 % des patients atteints de STOP souffriraient de migraine, 20 %–30 % répondent aux critères diagnostiques du syndrome d’Ehlers–Danlos de type hypermobile ou d’un trouble du spectre de l’hypermobilité23, et environ 15 % ont une comorbidité autoimmune. Une revue des études ayant analysé les taux de STOP et d’autres formes d’intolérance orthostatique chez les patients souffrant du syndrome d’Ehlers–Danlos ont conclu que l’intolérance orthostatique et la tachycardie affectaient 35 %–50 % des patients présentant un trouble du spectre de l’hypermobilité24. Certains patients atteints de STOP ont des symptômes qui font penser à une activation mastocytaire anormale. Ces patients font état de bouffées vasomotrices, d’urticaire, de dyspnée, de céphalées et de symptômes gastrointestinaux, comme la diarrhée, les nausées et les vomissements25. Un trouble du spectre de l’hypermobilité peut coexister avec un trouble de l’activation mastocytaire chez certains patients atteints de STOP.
Lorsqu’ils consultent pour la première fois, les patients atteints de STOP se font souvent dire à tort qu’ils souffrent d’un trouble anxieux. Dans un sondage d’envergure mené auprès de patients atteints de STOP, 77 % des répondants se sont fait dire qu’ils souffraient d’un trouble de santé mentale ou psychologique avant que l’on diagnostique leur STOP, et cette proportion diminuait à 37 % après leur diagnostic4. Ces faux diagnostics découlent probablement du fait qu’on associe parfois l’anxiété à la tachycardie, aux palpitations et aux étourdissements.
Quelle est la physiopathologie du STOP?
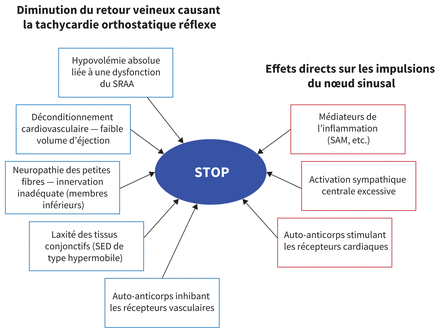
La figure 1 présente certains mécanismes physiopathologiques potentiels du STOP. La plupart des patients atteints ont un faible volume d’éjection systolique26 qui peut provoquer une tachycardie sinusale. Les caractéristiques décrites dans des sous-groupes de patients incluent une stimulation du système nerveux sympathique (c.-a-d., STOP hyperadrénergique)17, dénervation sympathique périphérique partielle entraînant une hypovolémie centrale relative (c.-a-d., STOP neuropathique)27 et un faible volume sanguin (c.-a-d., hypovolémie absolue)28 qui peuvent être à l’origine de certaines autres caractéristiques hémodynamiques. Les signes d’hyperadrénergisme peuvent inclure tremblements, anxiété, migraine et douleurs rétrosternales pseudo-angineuses22. Certains dérèglements du système nerveux autonome, particulièrement le système nerveux sympathique, sont primaires (c.-a-d., STOP hyperadrénergique central), d’autres sont secondaires à une autre anomalie physiologique (p. ex., hypovolémie).
Mécanismes physiopathologiques proposés pour expliquer le syndrome de tachycardie orthostatique posturale (STOP). Les cases bleues correspondent aux processus susceptibles d’entraîner une baisse du volume sanguin circulant, un ralentissement du retour veineux en position debout et une tachycardie orthostatique réflexe. Les cases rouges correspondent aux principaux processus qui affectent la réponse du nœud sinusal aux changements orthostatiques et la réponse chronotrope anormale en position debout. Différents mécanismes peuvent se recouper. Par exemple, les auto-anticorps qui ciblent les récepteurs cardiaques peuvent entraîner une réponse anormale durant l’orthostase, tandis que ceux qui ciblent les récepteurs vasculaires peuvent entraîner une stase veineuse, une hypovolémie relative et une tachycardie réflexe en position debout. Remarque: SAM = syndrome d’activation mastocytaire, SED = syndrome d’Ehlers–Danlos, SRAA = système rénine–angiotensine–aldostérone.
Le syndrome de tachycardie orthostatique posturale peut avoir une étiologie immunologique. De nombreux patients décrivent un déclenchement postinfectieux29–32 et 15 %–20 % des patients atteints de STOP ont des antécédents de troubles autoimmuns, comme la thyroïdite de Hashimoto, la polyarthrite rhumatoïde ou le syndrome de Sjögren4. Récemment, de nombreux cas de STOP33 et d’autres formes de tachycardie sinusale (p. ex., tachycardie sinusale inappropriée)34 ont été rapportés après une infection au SRAS-CoV-2. On ne dispose pas de bonnes données sur la fréquence du STOP chez les patients qui souffrent de complications à long terme de la COVID-19 (« syndrome post-COVID-19 »). Les auto-anticorps dirigés contre les récepteurs membranaires couplés aux protéines G cardiovasculaires intéressent particulièrement la recherche, mais leur rôle dans la physiopathologie du STOP reste à élucider35.
Les caractéristiques cliniques de la neuropathie des petites fibres ont de tout temps été utilisées pour le diagnostic de la neuropathie autonome partielle. Certains patients atteints de STOP présentent de l’α-synucléine phosphorylée dans leurs biopsies cutanées36, ce qui évoque un mécanisme neuropathique potentiellement lié à la maladie de Parkinson et l’insuffisance autonome pure.
La prévalence accrue du STOP parmi les membres d’une même famille permet de supposer une prédisposition génétique. À une exception notable près concernant une mutation particulière responsable du STOP chez les membres d’une même famille37, aucune donnée n’appuie l’étiologie monogénique du STOP.⇓
Approche initiale suggérée pour le traitement du syndrome de tachycardie orthostatique posturale
Traitements non pharmacologiques
Tous débutés dès la visite initiale
Eau 3 L/j
Sel 5 mL/j
Vêtements de compression montant jusqu’à la taille
Traitements pharmacologiques
Peuvent débuter dès la visite initiale si les symptômes sont importants
Si la fréquence cardiaque en position debout est très élevée: propranolol 10–20 mg, 4 fois par jour
Si la fréquence cardiaque en position debout est très élevée et que les β-bloquants sont contre-indiqués: ivabradine 5 mg 2 fois par jour
Si la fréquence cardiaque en position debout n’est pas trop élevée et que la tension artérielle est basse: midodrine 5 mg par voie orale toutes les 4 h, 3 fois par jour (8 h, midi, 16 h)
Remarque: c. à thé: cuillère à thé.
Traitements pharmacologiques pour le syndrome de tachycardie orthostatique posturale
Comment fait-on le dépistage du STOP?
Lorsqu’ils soupçonnent un STOP, les médecins devraient procéder à une anamnèse, réaliser un examen physique, notamment mesurer les signes vitaux orthostatiques à intervalles réguliers après l’adoption de la station debout (en notant les symptômes associés) et demander un électrocardiogramme à 12 dérivations. Une surveillance Holter de 24 heures peut permettre de déceler la présence d’une tachycardie sinusale inappropriée. Cette approche minimale suffit habituellement pour poser un diagnostic et instaurer le traitement. Il y a une pénurie de médecins experts en traitement du STOP dans la plupart des régions canadiennes, mais l’évaluation initiale peut être effectuée en médecine de soins primaires et en pédiatrie. Si les patients présentent une réponse insatisfaisante ou inadéquate au traitement initial, il faut envisager une consultation auprès d’experts du STOP.
La vérification des antécédents médicaux devrait être axée sur les causes sous-jacentes possibles et les troubles associés, les facteurs et événements déclencheurs potentiels du STOP, la gravité des symptômes, les facteurs qui atténuent ou aggravent les symptômes, la capacité fonctionnelle des patients et l’impact de leurs symptômes sur leur qualité de vie. Les médecins devraient poser des questions sur les symptômes pouvant faire penser à une dysfonction autonome, comme les troubles gastrointestinaux ou urinaires, la diaphorèse anormale, l’acrocyanose, la sécheresse buccale et une fièvre inexpliquée. La plupart des patients se plaignent de céphalées, le plus souvent de migraines. Ils font également souvent état d’une alternance entre diarrhée et constipation. Un nombre substantiel de patients mentionne des symptômes affectant la motilité gastrique, soit nausées et vomissements, qui peuvent limiter l’apport alimentaire et hydrique. Ces patients parlent alors de nausées qui s’aggravent à la station debout et qui répondent au traitement de la tachycardie. Certains patients se plaignent de symptômes de dysfonction vésicale (incontinence ou impériosité). Les problèmes de paresthésie et d’engourdissements des membres peuvent suggérer une neuropathie des petites fibres, car les nerfs du système autonome sont de petit calibre. L’intolérance au chaud et au froid est souvent mentionnée. La plupart des patients se plaignent de dysfonction cognitive subjective (« brouillard cérébral ») et de fatigue envahissante. Les médecins devraient faire une revue attentive des médicaments, car certains peuvent aggraver les symptômes, et vérifier si l’apport sodé et hydrique est adéquat.
La fréquence cardiaque et la tension artérielle doivent être mesurées lorsque le patient est en position couchée depuis 5–10 minutes pour permettre l’équilibration des liquides, et ensuite, 1, 3, 5, 8 et 10 minutes après l’adoption de la station debout5. Pour diagnostiquer une tachycardie orthostatique excessive (nécessaire au diagnostic du STOP), les patients doivent présenter une accélération soutenue de leur fréquence cardiaque d’au moins 30 battements/min (chez les adultes) ou d’au moins 40 battements/min (chez les patients de 12–19 ans) à au moins 2 reprises en position debout. La tension artérielle systolique ne devrait pas diminuer de plus de 20 mm Hg.
Étant donné la variabilité diurne substantielle (la fréquence cardiaque étant plus élevée en position debout et la tachycardie orthostatique se manifestant le matin), les évaluations matinales seront probablement plus sensibles11. Le test de la table basculante (pendant au moins 10 min), idéalement avec un monitorage de la tension artérielle continu avec chaque pulsation38, n’est pas indispensable, mais il peut aussi aider au diagnostic du STOP. Le test de la table basculante donne lieu à une accélération de la fréquence cardiaque légèrement plus marquée que le test de la position debout39, ce qui en accroît la sensibilité diagnostique. Le test de la table basculante est souvent utilisé dans les centres spécialisés, car on peut la combiner avec un monitorage plus précis.
En plus des signes vitaux orthostatiques, l’examen physique devrait inclure une évaluation de l’hypermobilité articulaire si on soupçonne le syndrome d’Ehlers–Danlos ou si le patient se dit hyperflexible23,40. L’auscultation cardiaque peut révéler des signes de prolapsus de la valvule mitrale. Certains patients atteints d’acrocyanose déclive peuvent présenter une décoloration bleutée des pieds et des mollets lorsqu’ils sont debout, la peau étant fraîche au toucher.
Footnotes
Intérêts concurrents: Satish Raj bénéficie de subventions de recherche des Instituts de recherche en santé du Canada (bourse MOP142426), de Dysautonomia International et de l’Institut Vanderbilt pour la recherche clinique et translationnelle, soutenue par une bourse en sciences cliniques et translationnelles du National Center for Advancing Translational Sciences des National Institutes of Health (UL1 TR000445). Il déclare avoir reçu des honoraires à titre de consultant de Lundbeck, Theravance Biopharma et ArgenX BV et une rémunération ou des honoraires de Medscape, Spire Learning, Academy for Continued Healthcare Learning et Autonomic Neurosciences. Il signale également avoir été rémunéré en tant qu’expert témoin par Faris Law, et pour sa participation à des comités de surveillance de la sécurité des données d’Arena Pharmaceuticals et sa participation sans rémunération aux conseils de l’American Autonomic Society et de l’Académie de la Société canadienne de cardiologie. Artur Fedorowski bénéficie d’une subvention de recherche de Dysautonomia International. Il signale avoir reçu des honoraires à titre de consultant d’ArgenX BV et une rémunération ou des honoraires de Biotronick, Finapres Medical Systems et Bristol Myers Squibb. Il signale en outre avoir perçu des frais de consultation, des honoraires et avoir participé à un comité de surveillance de la sécurité des données de Medtronic. Robert Sheldon bénéficie d’une subvention de recherche des Instituts de recherche en santé du Canada et de Dysautonomia International. Il signale aussi avoir 3 brevets en instance en lien avec la surveillance de la tension artérielle et il participe à un comité de surveillance de la sécurité des données pour un essai clinique sur la fibrillation auriculaire.
Cet article a été commandé et a été révisé par les pairs.
Collaborateurs: Tous les auteurs ont contribué à la conception du travail, ont rédigé le manuscrit, en ont révisé de façon critique le contenu intellectuel important; ils ont donné leur approbation finale pour la version destinée à être publiée et assument l’entière responsabilité de tous les aspects du travail.
This is an Open Access article distributed in accordance with the terms of the Creative Commons Attribution (CC BY-NC-ND 4.0) licence, which permits use, distribution and reproduction in any medium, provided that the original publication is properly cited, the use is noncommercial (i.e., research or educational use), and no modifications or adaptations are made. See: https://creativecommons.org/licenses/by-nc-nd/4.0/